Наукова робота. Визначення концентрації вуглекислого газу у повітрі
02.6k Поширити
Підготувала:
Лемішко Мар’яна,
учениця 10-Б класу
СЗШ №13 м. Львова
Керівник:
Жировецька Людмила Емерихівна,
вчителька хімії
СЗШ №13 м. Львова,
лауреатка IV Всеукраїнського Інтернет-конкурсу
„УЧИТЕЛЬ РОКУ–2019” за версією
науково-популярного природничого журналу
„КОЛОСОК” у номінації „Хімія”
ВСТУП
Актуальність. Сьогодні тривалий час людина перебуває в приміщенні: школярі у класах, студенти в аудиторіях, дорослі проводять на робочих місцях до восьми робочих годин. В приміщенні, де багато людей, важке повітря. Виникає відчуття, що не вистачає кисню. Проте, насправді це зовсім не так. Концентрація кисню в повітрі відповідає нормі, а концентрація вуглекислого газу значно підвищена. Які зміни проходять в організмі людини? Наскільки це шкідливо?
Об’єкт дослідження: повітря в класних кімнатах.
Предмет дослідження: концентрація вуглекислого газу в повітрі.
Мета роботи: навчитися визначати концентрацію вуглекислого газу.
Завдання:
- Опрацювати літературні джерела про роль вуглекислого газу.
- Дослідити концентрацію вуглекислого газу у класі кімнаті перед початком і в кінці уроку.
- Порівняти значення концентрації вуглекислого газу на шкільному подвір’ї з отриманими даними в результаті дослідження.
- Узагальнити результати дослідження, скласти звіт про виконану роботу.
- Виробити практичні рекомендації щодо дотримання оптимального повітряного режиму в приміщенні.
Методи дослідження:
– теоретичні (робота з різними джерелами інформації );
- дослідницький експеримент.
Практичне значення
Результати досліджень можна використовувати для визначення чи прогнозування якості повітря у класних кімнатах.
РОЗДІЛ 1. ЗНАЧЕННЯ ВУГЛЕКИСЛОГО ГАЗУ У ЖИТТІ ЛЮДИНИ
1.1 Роль вуглекислого газу в життєдіяльності організму
Вуглекислий газ має таке ж важливе значення для організму, як і кисень. Він є фізіологічним стимулятором дихання: впливає на кору головного мозку і стимулює дихальний центр. Сигналом для чергового вдиху є не нестача кисню, а надлишок вуглекислого газу.
Розглянемо механізм дихання. При вдихові легені наповнюються киснем. В альвеолах легень проходить газообмін : кисень поступає в кров, а вуглекислий газ виділяється з неї. Потім людина видихає. СО2 – один з кінцевих продуктів метаболізму. Людина вдихає до 30 літрів кисню на годину і видихає 20-25 літрів вуглекислого газу.
Вуглекислий газ відіграє важливу роль в підтримуванні кислотно-лужної рівноваги, у біосинтезі білка, впливає на вироблення гормонів, активність ферментів і швидкість біохімічних процесів. Він бере участь у розподілі іонів натрію в тканинах, регулює збудливість нервових клітин, впливає на проникність клітинних мембран, активність багатьох ферментів, інтенсивність продукування гормонів і ступінь їх фізіологічної ефективності, процес зв’язування білками іонів кальцію і заліза.
Норма вуглекислого газу в крові – 7-7,5 % , а в альвеолярному повітрі – 6,5 %. Отримати вуглекислий газ з повітря, яким дихає людина, практично не можливо, бо в атмосферному повітрі він міститься у мізерних кількостях. До людського і тваринного організму він поступає як кінцевий продукт при повному розщепленні їжі ( білків, жирів, вуглеводів).
1.2 Вплив підвищеної концентрації вуглекислого газу в повітрі на здоров’я людини
Хімічний склад повітря має важливе гігієнічне значення і відіграє вирішальну роль у здійсненні дихальної функції організму. Атмосферне повітря містить 20,94% кисню, 0,04% вуглекислого газу, 78,08% азоту, 0,94% – інші гази. У видихуваному повітрі вміст кисню становить 15,4-16%, вуглекислого газу – 3,4-4,7%, азоту – 78,26%, інші гази – 0,94%.
Гігієнічне значення вуглекислого газу полягає в тому, що за його концентрацією в повітрі роблять висновок про чистоту або забрудненість цього повітря. Якщо в невеликій кімнаті при поганій вентиляції або при її відсутності перебуває багато людей концентрація вуглекислого газу може значно перевищити норму. Людина зразу ж починає відчувати симптоми «нестачі свіжого повітря» (а насправді підвищеної концентрації вуглекислого газу) уже при його рівні 0,08%. В результаті може виникнути головний біль, нудота, сонливість, закладення носа, подразнення горла і очей.
Незадовільна якість повітря в класних кімнатах та кабінетах негативно відбивається на результативності навчання. На кінець кожного уроку повітря в класі стає «задушливим».
Зниження вмісту СО2 в атмосферному повітрі не викликає небезпеки для організму людини тому, що показник вмісту вуглекислого газу в крові підтримується регуляторними механізмами організму людини. А коли підвищується концентрація СО2 в атмосферному повітрі – це викликає порушення діяльності організму. Повітря вважається токсичним при концентрації СО 2 – 2,5%. При 3-% концентрації вуглекислого газу в атмосферному повітрі у людини прискорюється і поглиблюється дихання, підвищується серцебиття, а при 8-% концентрації СО2 в атмосферному повітрі настає важке отруєння і смерть.
РОЗДІЛ 2. ЕКСПРЕС-МЕТОД ВИЗНАЧЕННЯ ВУГЛЕКИСЛОГО ГАЗУ В ПОВІТРІ
Прилади і матеріали: шприц об’ємом 100 мл, хімічна склянка, 20 мл 0,005% водного розчину натрій карбонату з фенолфталеїном.
Порядок виконання експерименту
- 1. Приготування 0,005 %-й розчин натрій карбонату.
1 г хімічно чистого безводного натрій карбонату розчиняємо у 200 мл дистильованої води, а потім додаємо 0,5 мл 1 %-го розчину фенолфталеїну.
Оскільки розчин має лужну реакцію внаслідок гідролізу:
Na₂CO₃ + H₂O → H₂CO₃ + 2NaOH
2Na⁺ + CO₃2- + H⁺ + OH– → 2Na⁺ + 2OH– + H₂CO₃,
то фенолфталеїн (pH 8-10) забарвлює розчин у малиновий колір (Рис. 2.1)
- Приготування робочого розчину.
1мл 0,005 %-го розчину Na2СO3 поміщаємо в мірну колбу на 100 мл, доводимо об’єм дистильованою водою до позначки й ретельно перемішуємо.
- В медичний шприц на 100 мл набираємо 20 мл робочого розчину Na2СO3, потім відтягуємо поршень до позначки 100 мл, засмоктуючи досліджуване повітря, після чого активно струшуємо протягом 1 хв. Якщо розчин не знебарвлюється, набираємо нову порцію повітря, перед тим виштовхуючи попередню й залишаючи в шприці той же об’єм Na2СO3, струшуємо протягом 1 хв. (Рис 2.2). Так повторюємо, доки забарвлення не зникне (лужне → нейтральне):
Na₂CO₃ + H₂O + CO2 → 2NaHCO₃ + 2H⁺.
- Об’єм повітря, яке пройшло через шприц, дає змогу визначити концентрацію СО₂ за таблицею 2.1(додаток 1).
РОЗДІЛ 3. РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ
Дослідженнями підтверджено: вміст вуглекислого газу в повітрі є величиною сталою 0,04%. Об’єм повітря, який був засмоктаний шприцом на шкільному подвір’ї – становив 520 мл. (Рис.3.1)
Отримані експериментальні дані вказують на те, що концентрація СО2 у приміщенні залежить від кількості осіб, часу перебування й санітарно-гігієнічних умов (Табл.3.1 ) (додаток 2)
ВИСНОВКИ
- В результаті дослідження зміни концентрації вуглекислого газу в приміщенні та на шкільному подвір’ї встановлено, що концентрація вуглекислого газу на подвір’ї – величина стала – 0,04 %, а у класній кімнаті перебуває у прямо пропорційній залежності від часу перебування учнів у класній кімнаті.
- Вуглекислий газ служить непрямим показником антропогенного забруднення повітря приміщень, критерієм ступеня чистоти повітря, за яким можна судити про санітарний стан повітря приміщень.
- Незадовільна якість повітря може негативно позначається на самопочутті учнів і на їхній продуктивності праці під час уроку. Щоб домогтися необхідної якості повітря в класах, потрібно:
– провітрювати приміщення на перервах;
– залишати вікна трохи прочиненими і під час уроку;
– здійснювати вологе прибирання в класній кімнаті між уроками і після уроків.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Білявський Г.О., Фурдуй Р.С. Основи екологічних знань: підручник. – К.: Либідь, 1997. – 288 с.
- Бойчук Ю.Д., Солошенко Е. М. Екологія і охорона навколишнього середовища. – К.: Видавничий дім «Княгиня Ольга», 2005. – 302 с.
- Джигирей В. С. Екологія та охорона навколишнього природного середовища: навч. посібник. -К.: Знание, КОО., 2004. – 309 с.
- Задорожний К.М. Усі уроки екології. 11 клас. Проф. рівень / К.М. Задорожний, О.Г. Стадник – Х.: “Основа”, 2011. – 363 с.
- Задорожний К.М. Усі уроки екології. 10 клас. Проф. рівень / К.М. Задорожний, В.І. Садкіна. – Х.: “Основа”, 2010. – 381 с.
- Зелений пакет. Посібник для вчителя. Посібник рекомендовано Міністерством освіти і науки України для використання у загальноосвітніх навчальних закладах України (Наказ Міністерства освіти і науки України від 07.12.2009 року№1/11-9999)
- Корсак К.В., Плахотнік О.В. Основи екології, – К.: МАУП, 2000. – 238 с.
- Природа. Екологія. Для дітей середнього шкільного віку / А.А. Ходоренко – Х.:Фоліо, 2008. – 315 с.
- Царик Л.П. Екологія: підручник для 11 класу загальноосвітніх навчальних закладів. Рівень стандарту, академічний рівень / Л.П. Царик, П.Л. Царик, І.М. Вітенко – К.: Генеза, 2012. – 96 с. іл.
- Сайт studepedia.org Методична вказівка до практичного заняття з гігієни для студентів 3 курсу фармацевтичного факультету
Додаток 1
Таблиця 2.1
Залежність вмісту СО2 в повітрі від об’єму повітря, що знебарвило 20 мл 0,005 % розчину соди
|
Об’єм повітря, мл |
Концентрація СО2 , % |
Об’єм повітря, мл |
Концентрація СО2, % |
Об’єм повітря, мл |
Концентрація СО2, % |
|
80 |
0,320 |
330 |
0,116 |
410 |
0,084 |
|
160 |
0,208 |
340 |
0,112 |
420 |
0.080 |
|
200 |
0,182 |
350 |
0,108 |
430 |
0,076 |
|
240 |
0,156 |
360 |
0,104 |
440 |
0,070 |
|
260 |
0,144 |
370 |
0,100 |
450 |
0,066 |
|
280 |
0,136 |
380 |
0,096 |
460 |
0,060 |
|
300 |
0,128 |
390 |
0,092 |
480 |
0,052 |
|
320 |
0,120 |
400 |
0,088 |
520 |
0,040 |
Додаток 2
Табл.3.1
Залежність концентрації СО2 від різних чинників ( кількості осіб і санітарно-гігієнічного стану приміщення)
|
|
Об’єм повітря (мл) |
Вміст СО₂ (%) |
|
1 проба (шкільне подвір’я) |
520 |
0,040 |
|
2 проба ( після 1 уроку, 25 учнів) |
480 |
0,052 |
|
3 проба ( після 7 уроку, 25 учнів) |
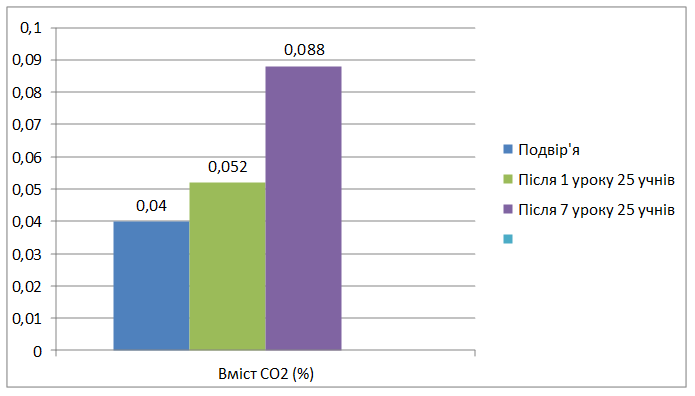
400 |
0,088 |
Отримані числові значення відобразили діаграмою ( Рис. 3.2 )
Редакція може не поділяти думку авторів і не несе відповідальність за достовірність інформації. Будь-який передрук матеріалів з сайту може здійснюватись лише при наявності активного гіперпосилання на e-kolosok.org, а також на сам матеріал!
Схожі публікації
КОЛОСОК ДЛЯ ЗСУ 9-11 клас
Запрошуємо до участі у конкурсі усіх великих і малих ))), і не думайте що якщо Ви великі, то вам буде легко )
КОЛОСОК ДЛЯ ЗСУ 7-8 клас
Запрошуємо до участі у конкурсі усіх великих і малих ))), і не думайте що якщо Ви великі, то вам буде легко )
КОЛОСОК ДЛЯ ЗСУ 5-6 клас
Запрошуємо до участі у конкурсі усіх великих і малих ))), і не думайте що якщо Ви великі, то вам буде легко )