Роботу виконав:
Іманов Даніїл Тагірович
учень 8 класу
ЗЗСО І-ІІІ ступенів №16
ВЦА м. Торецьк
Донецької області
Науковий керівник:
Коріненко Світлана Іванівна
вчителька біології та географії
ЗЗСО І-ІІІ ступенів №16
ВЦА м. Торецьк
Донецької області
лауреатка IV Всеукраїнського Інтернет-конкурсу
„УЧИТЕЛЬ РОКУ–2019” за версією
науково-популярного природничого журналу
„КОЛОСОК” у номінації „ХІМІЯ”
ВСТУП
Вода є необхідною умовою і складовою частиною життя на Землі. Здоров’я та благополуччя людей значною мірою залежить від водних ресурсів. У результаті глобального техногенного впливу на природу вода, як її вагома життєдайна складова, зазнала і зазнає значних змін, що негативно впливають на діяльність та здоров’я людей. За даними Всесвітньої Організації Охорони Здоров’я (ВООЗ), щороку у світі біля 25% населення піддається ризику споживання неякісної питної води, до складу якої входять речовини, що можуть викликати токсичні, мутагенні та канцерогенні ефекти. Основними проблемами екології, які пов’язані з гідросферою планети, є умови забезпечення населення водою, її якістю та можливості її підвищення. До недавнього часу ці проблеми не стояли так гостро, в зв’язку з відносною чистотою природних джерел водопостачання та їх достатньою кількістю. Але в останні десятиріччя ситуація різко змінилася.
Значна концентрація міського населення, різке збільшення промислових, транспортних, сільськогосподарських, енергетичних та інших антропогенних викидів призвели до порушення якості води, появі в джерелах водопостачання невластивих природному середовищу хімічних, серед яких значне місце посідають фосфати), радіоактивних та біологічних агентів. Найбільше фосфатів у навколишнє середовище надходить із стічними водами та побутовими відходами людини. Все це робить ефективне водозабезпечення населення провідною проблемою сучасної гігієни. Експертами ВООЗ встановлено, що 80% всіх хвороб в світі пов’язано з незадовільною якістю питної води та порушенням санітарно-гігієнічних та екологічних норм водозабезпечення.
Метою дослідження є визначення якості питної води в смт Новгородське Донецької області.
Поставлена мета передбачає виконання таких завдань:
- опрацювати літературні та інтернет-джерела з досліджуваної теми;
- вивчити проблеми якості питної води;
- опрацювати методику щодо відбору проб води для аналізів;
- дослідити якість питної води, а саме: колір, прозорість, запах, твердість;
- провести анкетування серед жителів селища Новгородське.
Після проведення анкетування серед жителів селища були отримані наступні результати:більша частина населення споживає воду централізованого водогону (38%),фасовану воду споживають 29%, воду зі свердловини 27%, з інших джерел -5%.
Об’єкт дослідження: питна вода в селищі Новгородське.
Предмет дослідження: якість питної води з водогону, джерела в районі ставка, криниці.
Для вирішення цих завдань були використані такі методи: теоретичний аналіз літератури та інших джерел інформації, присвячених проблематиці дослідження; лабораторні дослідження води з водогону, джерела в районі ставка, криниці в районі Верхнього Кераму.
РОЗДІЛ 1. ГІГІЄНІЧНІ ВИМОГИ І НОРМАТИВИ ЯКОСТІ ПИТНОЇ ВОДИ
Якість питної води служить основою епідемічної безпеки і здоров’я населення. Доброякісна вода є показником високого санітарного благополуччя і життєвого рівня населення, забезпеченого централізованим водопостачанням. У розвинених країнах якості питної води держава та органи охорони здоров’я приділяють особливу увагу.
Питна вода повинна відповідати СанПіН 2.1.4.1074-01 «Питна вода. Гігієнічні вимоги до якості води централізованих систем питного водопостачання. Контроль якості». Дані санітарні правила застосовуються щодо води, призначеної для споживання населенням в питних і побутових цілях, для використання в процесах переробки продовольчої сировини та виробництва харчових продуктів, їх зберіганні і торгівлі, а також для виробництва продукції, що вимагає застосування води питної якості. Питна вода, що реалізується населенню в бутлях, контейнерах, пакетах, повинна відповідати вимогам СанПіН 2.1.4.1116-02 «Питна вода. Гігієнічні вимоги до якості води, розфасованої в ємності. Контроль якості».
Питна вода повинна мати сприятливі органолептичні властивості, нешкідлива за хімічним складом, бути безпечна в епідемічному й paдіаціонном відношенні.
1.1. Органолептичні показники якості води
До органолептичних показників води відносяться: запах, присмак, кольоровість, каламутність, прозорість.
Запахи природного походження обумовлені живуть і отмирающими у воді організмами, впливом берегів, дна, грунтів, грунтів і т.д. Так, присутність у воді рослинних залишків надає їй землистий, мулистий або болотний запах; при цвітінні вода має ароматичний запах; наявність сірководню надає воді запах тухлих яєць; при гнитті органічних речовин або забрудненні її нечистотами виникає гнильний, сірководневий або фекальний запах.
Запахи штучного походження виникають при забрудненні води промисловими та іншими стічними водами (фенольний, камфорний, аптечний, хлорний, металевий, бензиновий і т.п.).
Інтенсивність запаху питної води оцінюється за 5-ти бальною системою, представленої в табл. 1. Запах води не повинен перевищувати 2-х балів.
Таблиця 1.1.1. Оцінка інтенсивності запаху
|
Інтенсивність запаху |
Характер прояву запаху |
Інтенсивність, балів |
|
Немає |
Запах не відчувається |
0 |
|
Дуже слабка |
Запах не відчувається споживачем, але виявляється при лабораторному дослідженні |
1 |
|
Слабка |
Запах виявляється споживачем, якщо звернути на це увагу. |
2 |
|
Помітна |
Запах легко помічається та викликає негативні відгуки |
3 |
|
Виразна |
Запах звертає на себе увагу і змушує утриматись від споживання води. |
4 |
|
Дуже сильний |
Запах настільки сильний,що робить воду непридатною для використання. |
5 |
Смак і присмак. Питна вода повинна бути приємною, мати освіжаючий смак без будь-якого стороннього присмаку. Смак води залежить від мінерального складу води, температури її і розчинених газів. Розрізняють чотири основних смакових відчуття: солоне, кисле, солодке, гірке. Всі інші смакові відчуття називаються присмаками (лужний, металевий, хлорний, терпкий і т.д.). Визначення смаку і присмаку проводиться у свідомо безпечної води при температурі 200 С, а в сумнівних випадках воду кип’ятять протягом 5 хв і охолоджують.
Гігієнічне значення запахів і присмаків води полягає в тому, при їх інтенсивності вище 2 балів обмежується водоспоживання; штучні запахи і присмаки можуть бути показниками забруднення води стічними водами; природні запахи і присмаки вище 2 балів свідчать про наявність у воді біологічно активних речовин, що виділяються синьо-зелених водоростей. Кольоровість – природну властивість води, обумовлене наявністю гумінових речовин, які утворюються при руйнуванні органічних сполук у грунті, вимиваються з неї, надходять у відкриті водойми і надають їм забарвлення від жовтуватого до коричневого кольору.
Тому кольоровість властива воді відкритих водойм і різко збільшується в паводковий період. Забарвлення воді можуть надавати сполуки заліза (жовто-зеленувате фарбування), квітучі водорості, завислі речовини, забруднення стічними водами та ін. Кольоровість питної води визначають фотометричним шляхом, вона не повинна бути вище 20о, тоді вода вважається безбарвною.
Гігієнічне значення кольоровості полягає в тому, що при кольоровості вище 35о обмежується водоспоживання; збільшення або зменшення кольоровості підземних вод свідчить про їх забрудненні; кольоровість є показником ефективності знебарвлення води на водопровідних спорудах.
Каламутність води залежить від наявності у воді зважених частинок мінерального або органічного походження. Підвищена каламутність обмежує водоспоживання, свідчить про забруднення природних вод. Каламутність є показником ефективності процесу освітлення води на очисних спорудах.
1.2. Хімічний склад води
До хімічних показників відносяться: водневий показник (рН), окисно-відновний потенціал, загальна мінералізація (сухий залишок), жорсткість, мікроелементи, іонний склад, радіоактивні речовини.
До хімічних речовин, здатним погіршити органолептичні властивості води, належать природні мінеральні елементи (хлориди, сульфати, залізо, мідь, цинк, солі кальцію і магнію), а також деякі хімічні речовини, що додаються до питної води в процесі її обробки. Зміна органолептичних показників води справляє негативний вплив на людину і може привести до погіршення санітарного стану води (наприклад, підвищення каламутності води знижує бактерицидну дію хлорування).
Жорсткість води знижує смакові достоїнства і засвоюваність приготовленої їжі. Так, овочі і м’ясо, зварені в жорсткій воді, погано перетравлюються в результаті утворення важкорозчинних сполук білка з солями кальцію і магнію; погіршуються вигляд і смак чаю. Жорстка вода утворює нерозчинний осад на трубах гарячого водопостачання і посуді, ускладнюючи догляд за ними. Виявлено зв’язок між вживанням жорсткої води і підвищеною захворюваністю сечокам’яною хворобою. Допустима жорсткість води не повинна перевищувати 7 мг / екв / л.
До числа природних хімічних речовин, що мають велике фізіологічне значення відносяться фтор. Так, при підвищеному вмісті фтору в грунті і, отже, у воді (більше 1,5 мг / л) розвивається захворювання флюороз, зовнішньою ознакою якого є поява плям на зубній емалі; при вмісті фтору в кількості менше 0,5 мг / л виникає карієс зубів.
У СанПіН 2.1.4.1116-02 «Питна вода. Гігієнічні вимоги до якості води, розфасованої в ємності »включені також норми ГДК для ряду хімічних речовин, найбільш небезпечних для здоров’я людини, таких як берилій, ртуть, свинець, молібден, миш’як, стронцій та інші, які можуть стати причиною хронічних інтоксикацій людини. ГДК цих елементів у питній воді визначені в залежності від ступеня їх токсичної дії і кумулятивних властивостей (здатності до накопичення в організмі).
З числа можливих хімічних забруднювачів питної води важливе гігієнічне значення мають нітрати. Нітрати можуть міститися в глибоких підземних водах як їх природний компонент, проте основним джерелом накопичення нітратів у водоймах є продукти розкладу органічних речовин стічних вод. Отже, кількість нітратів у воді служить непрямим показником забруднення її органічними речовинами побутового походження. Значення нітратів, як санітарного показника якості води, а також їх токсичність (розвиток метгемоглобінемії у дітей) при значному підвищенні концентрації нітратів послужили підставою для їх обмеження в питній воді (до 45 мг / л по йону NO3–).
Вміст шкідливих хімічних речовин, що надходять і утворюються у воді в процесі її обробки в системі водопостачання. Ця група об’єднує токсичні речовини, присутність яких обумовлено додаванням реагентів з метою освітлення, знебарвлення та знезараження води або проведенням одного з видів спеціальної обробки (пом’якшення, фторування та ін.) Так, для очищення питної води використовується синтетичний органічний флокулянт – поліакриламід (ПАА), залишкові кількості якого в питній воді не повинні перевищувати 2 мг / л.
Розчинений кисень. Надходження кисню у водні об’єкти відбувається у процесі газообміну з атмосферою, фотосинтезу, зі стічними водами, зливовими і талими водами, які перенасичені киснем. Розчинений у воді кисень використовується гідробіонтами для дихання та окиснення органічних речовин. Низька концентрація розчиненого кисню негативно впливає на біохімічні та екологічні процеси у водному об’єкті. Концентрація кисню у поверхневих шарах вища, ніж у глибинних за рахунок посиленої поверхневої аерації та інтенсивного проходження процесів фотосинтезу.
Хімічне споживання кисню (ХСК). ХСК – це кількість кисню, необхідна для хімічного окиснення неорганічних і органічних речовин: вуглецевмісних – до СО2, Н2О, NН3; сірковмісних – до сульфатів, фосфоровмісних – до фосфатів. Органічні речовини потрапляють у поверхневі води з поверхневим стоком, скидами стічних вод.
Біохімічне споживання кисню (БСК). БСК – це кількість кисню, що витрачається за певний час на аеробне біохімічне окиснення нестійких органічних сполук до СО2, Н2О, NН3. Органічні речовини рослинного та тваринного походження надходять у воду з поверхневим стоком, скидами стічних вод. БСК визначають для різних проміжків часу: 5 діб інкубації мікроорганізмів – БСК5, 20 діб інкубації – БСК20; незалежно від часу для повного окиснення органічних сполук – БСКпов.
Водневий показник (рН). Вміст іонів водню у поверхневих водах визначається кількісним співвідношенням концентрацій вугільної кислоти та її іонів, геологічними особливостями водозбірного басейну річки. рН визначає ступінь її кислотності або лужності. Зміни pН тісно пов’язані з процесами фотосинтезу. Від розміру pН залежить розвиток і життєдіяльність водних рослин, сталість різноманітних форм міграції хімічних елементів, токсичність забруднюючих речовин. Більшість поверхневих вод має нейтральну або слабокислу реакцію (рН – від 6,0 до 8,0). Узимку величина pН для більшості річкових вод становить 6,8–7,4 од., улітку – 7,4–8,2 од. При значенні рН 4,0 – 6,0 од. у воді розвиваються гриби та дріжджі. Більшість бактерій обирають середовища, зі значеннями рН 6,5–7,5 од.
Сухий залишок. Сухий залишок – загальний вміст у воді нелетких органічних і мінеральних домішок у вигляді неорганічних (бікарбонати, хлориди та сульфати кальцію, магнію, калію і натрію) та деяких органічних солей, розчинних у воді. Концентрація сухого залишку залежить від геологічних особливостей водозбірного басейну річки, потрапляння вказаних солей зі скидами промислових стічних вод, зливовими водами.
Хлориди. Джерелами надходження хлоридів у поверхневі води є магматичні породи, до складу яких входять хлоровмісні мінерали, взаємодія атмосферних опадів з ґрунтами, скиди побутових і промислових стічних вод. Хлориди мають добру розчинність, слабо виражену здатність до сорбції завислими речовинами та споживання водними організмами. Вміст хлоридів визначає некарбонатну жорсткість води. Концентрація сульфатів піддається сезонним коливанням і залежить від вимивання з гірських порід у вигляді розчинних сполук.
Сульфати. Вміст сульфатів у поверхневих водах зумовлений процесами вивітрювання гірських порід, розчинення сірковмісних мінералів, окиснення сульфідів і сірки, відмирання водних організмів, окиснення речовин рослинного та тваринного походження, з підземним стоком, скидами шахтних вод, стічних вод галузей промисловості, житлово-комунального та сільського господарства. Вміст сульфатів визначає некарбонатну жорсткість води. Концентрація сульфатів піддається сезонним коливанням, так як вплив на їх вміст у воді мають окисно-відновні процеси, біологічна обстановка у водному об’єкті та господарська діяльність людини.
Фосфати. Джерелами потрапляння фосфатів у поверхневі води є ерозія орних земель, в яких містяться добрива, промислові відходи, побутові стічні води, які містять синтетичні миючі засоби та фекалії. Фосфати сприяють росту рослин і водоростей, збільшенню кількості фітопланктону та зоопланктону, збільшенню відмерлої біомаси. Фосфати є малотоксичними. Мінімальні концентрації фосфатів спостерігаються навесні і влітку, максимальні – восени і взимку.
Амоній сольовий. Джерелами надходження амонію сольового у поверхневі води пов’язано є скиди стічних вод тваринницьких ферм, скиди побутових стічних вод, стічних вод харчової лісохімічної та хімічної промисловості, поверхневий стік з сільськогосподарських угідь, в яких містяться амонійні добрива. Присутність амонію сольового пов’язана з процесами біохімічної деградації білків, дезамінування амінокислот, розкладу сечовини під дією уреази. Токсичність амонію збільшується з підвищенням pH.
Нафтопродукти. Нафтопродукти – органічні сполуки, отримані шляхом переробки нафти (автомобільне та дизельне паливо, гас, мастила, мазут). Вони потрапляють у поверхневі води зі скидами стічних вод нафтопереробних підприємств. Нафтопродукти можуть надходити до донних відкладень, перебувати в товщі води у вигляді емульсій, розчинятися в ній та утворювати на поверхні плівку у вигляді райдужних плям. Концентрації нафтопродуктів мають сезонні коливання залежно від гідрологічних особливостей басейну річки. Найбільше їх надходження спостерігається у зимову та літньо-осінню межень, найменше – під час проходження весняної повені та осінніх паводків.
Синтетичні поверхнево-активні речовини (СПАР). СПАР – це неорганічні та органічні речовини, що здатні утворювати піну на поверхні води. До цих речовин відносять миючі, зволожуючі, емульгуючі, дезінфікуючі та інші препарати. СПАР надходять у поверхневі води зі скидами побутовими стічних вод, скидами стічних вод нафтової та текстильної промисловості. Наявність СПАР у воді призводить до інтенсивного розвитку мікрофлори. Нижче населених пунктів у воді зазвичай спостерігається збільшення концентрацій СПАР. Найбільші концентрації СПАР спостерігаються під час весняного водопілля та літньо-осінніх паводків. Це пов’язано зі змивом їх з прилеглих територій та деякою мірою з температурою.[6]
1.3. Вплив забрудненої води на організм людини
Таблиця 1.3.1. Хвороби, що виникають при токсичному впливі домішок питної води.
|
Види забруднень |
Хвороби, що виникають |
|
Важкі метали: свинець, ртуть, кадмій, цинк, нікель, хром. метали: свинець, ртуть, кадмій, цинк, нікель, хром |
Атеросклероз, поліневрит, гіпертонія, ураження органів кровотворення (кістковий мозок), утрата гостроти зору. |
|
Неорганічні речовини: азот, фосфор |
Порушення імунітету людини |
|
Каналізаційні стоки: токсичні речовини, хвороботворні мікроорганізми. |
Хвороби травного тракту, менінгіт, поліомеліт, гепатит. |
|
Мінеральні добрива та ядохімікати: гербіциди, пестициди, нітрати, нітрити. |
Зараження води хвороботворною мікрофлорою. |
|
Хлорорганічні та неорганічні отруйні речовини. |
Ураження дітородної функції чоловіків та жінок, онкологічні захворювання, гепатити, ослаблення імунної системи. |
1.4. Значення рН води для життя і здоров´я людини
Як свідчать дослідження, мало хто з громадян обізнаний про кислотно-лужний баланс організму і його важливість не лише для здоров’я, а навіть і для життя. Тіло людини має певне кислотно-лужне співвідношення, що характеризується рН (водневий показник). Чим нижче рівень рН — тим середовище більш кисле (від 6.9 до 0), лужна ж середа має високий рівень рН (від 7.1 до 14). Тіло людини на 70% складається з води, тому вода — одна з найбільш важливих його складових. Тканини живого організму вельми чутливі до коливань показника pH. За межами певного діапазону (7.37-7.44) відбувається денатурація білків: руйнуються клітини, ферменти втрачають здатність виконувати свої функції, внаслідок чого можлива навіть загибель організму. Коли pH крові знижується, тіло починає накопичувати кислі речовини (зазвичай токсини) у клітинах, використовуючи клітини немов сміттєві баки, щоб врятувати кров від закислення. Клітини організму стають більш кислими і токсичними, що призводить до зменшення їх рівня кисню та пошкоджує їх ДНК.
Американські вчені зробили справжнє відкриття, коли виявили, що у будь-якого продукту, який ми вживаємо всередину, є фундаментальний показник, що має критичне значення для нашого життя. Це кислотне навантаження або кислотність їжі. Кислотне навантаження виражається співвідношенням в раціоні харчових компонентів, що в процесі переробки організмом утворюють кислоту або луг.
Більшість продуктів, що їх вживає в їжу середньостатистичний українець, підсилюють кислотне навантаження на організм. А зниження рівня рН в організмі в результаті “кислотного” харчування призводить до зниження імунітету і появи більш 200 захворювань, включаючи цукровий діабет, далекозорість та катаракту, хондроз і артроз, жовчно-та сечокам’яну хвороби, і навіть онкологічні захворювання. Якщо у людини почало проявлятися кілька захворювань одночасно — в наявності явне падіння рН крові і організму в цілому.
Ще в 1931 році Отто Варбург отримав Нобелівську премію з фізіології та медицини за визначення умов життя злоякісних пухлин. Клітини пухлин (а також бактерії і патогенні мікроорганізми) чудово розвиваються при закисленні крові, тобто при падінні рН нижче 7.2-7.3 одиниць. При нормалізації рН пухлини спочатку припиняли ріст, а потім розсмоктувалися!
Якщо рН крові в нормі, чужорідні бактерії і мікроорганізми просто не мають сприятливих умов для розмноження, оскільки всі клітини можуть жити і розмножуватися лише в діапазоні рН між 6.5 і 7.5. Здорові клітини мають рН 7.35, в той час як ракова клітина має більш кисле середовище. Тому коли рН злоякісної клітини піднімається вище 7.5 — вона починає вмирати, а якщо pH підвищується до рівня 8.0 — ракова клітина гине протягом декількох годин.[8]
Здавалося б, немає нічого простішого: треба їсти і пити більше тих продуктів, які мають вищий pH — і відсутність проблем зі здоров’ям людині гарантована. Але є одне “але”. Більшість продуктів, які ми вживаємо, мають низький, кислотний рівень pH. Наприклад, у картоплі він — 5.5, у м’яса — 3.5, у хліба — 5.5, у кави та чаю — 4-5, а пиво та газовані напої мають pH на рівні 2-3. В той час, як pH крові дорівнює 7.45, лімфи — 7.4, внутрішньосуглобової рідини — 7.3, міжклітинної рідини — 7.26-7.38…
Із вище сказаного роблю висновок – треба їсти більше сирих овочів та фруктів, меду, а також пити воду з підвищеним до рівня крові pH.
РОЗДІЛ 2. ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА
2.1. Результати опитування споживачів
До початку роботи я провів опитування серед своїх друзів та знайомих. Було з´ясовано, що мешканці нашого селища споживають бутильовану воду – 32 людини з опитаних, воду з системи централізованого водопостачання – 42, воду зі свердловини – 30, воду з інших джерел (наприклад, колодязну) – 6.
Результати опитування представлені діаграмою:
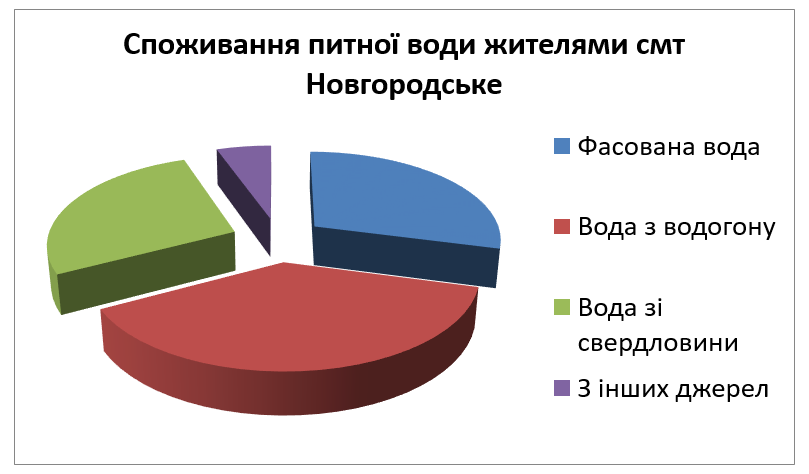
Діаграма 2.1.1
Тому для дослідження якості води я взяв три зразки води з наступних джерел:
№1 – вода з криниці (район Вернього Кераму).
вода з водогону; №2 – вода з джерела (район ставка); №3 – вода з водогону .
2.2. Визначення органолептичних показників води
Дослід №1. Визначення кольоровості води
Чиста вода безбарвна, а якщо вода має відтінок, то це означає, що вода непридатна для пиття. Присутність у воді розчиненого заліза і марганцю – така вода спочатку прозора, але при відстоюванні або нагріві набуває жовтувато – бурого забарвлення, що є причиною іржі патьоків на сантехніці. При підвищеному вмісті заліза вода також набуває характерного «залізистий» присмак.
Беремо пробірку і наливаємо в неї по черзі кожен з зразків і зі зворотного боку прикладаємо до них аркуш білого паперу.( Див. додаток А,Б)
Дослід №2. Визначення прозорості
Для визначення прозорості води використовуємо прозорий мірний циліндр з плоским дном, в який наливаємо воду, підкладаємо під циліндр на відстані 4 см від його дна шрифт, висота букв якого 2 мм, а товщина ліній букв – 0,5 мм. Зливаємо воду до тих пір, поки зверху через шар води не буде видно цей шрифт. Вимірюють висоту стовпа води, що залишилася лінійкою і висловлюють ступінь прозорості в см.(Див. додаток В)
Дослід № 3. Визначення запаху води.
Нагріваємо воду до 50-600С, для цього нам знадобиться термометр. Коли вода буде нагріта, за допомогою колових рухів визначаємо запах.
Результати дослідів №1,2,3 наведені у таблиці 2.2.1
Таблиця 2.2.1. Визначення органолептичних показників води в смт Новгородське
|
№ проби води |
Запах, балів |
Колір |
Прозорість |
|
№1 вода з криниці (район Вернього Кераму) |
2 |
Безбарвна |
32 см |
|
№ 2 вода з джерела (район ставка) |
Запах болотний 3 |
Жовтуватий |
27 см |
|
№3 вода з водогону |
1 |
Безбарвна |
30 см |
2.3. Визначення хімічного складу води
Дослід № 4. Визначення рН-показника
Для визначення рН-показника води я скористався універсальним індикатором. У пробірки зі зразками води опускав індикаторні папірці та оцінював їх колір. Результати представлені у таблиці 2.3.1(Див. додаток Г)
Таблиця 2.3.1. рН – показник досліджуваних проб води.
|
Проба води |
№1 вода з криниці (район Вернього Кераму) |
№ 2 вода з джерела (район ставка) |
№3 вода з водогону |
|
рН – показник |
6,5 |
6,5 |
7 |
Дослід № 5. Визначення жорсткості води
Для визначення жорсткості води використовую кип´ятіння впродовж 5-10 хвилин. Якщо вода містить солі Кальцію та Магнію, вони будуть випадати в осад.Усі три зразки мають підвищену жорсткість – при кип´ятінні утворився осад, схожий на накип у чайнику. Другий спосіб – до зразків води додаю шматочки мила, струшую впродовж 5 хвилин. Відстоюю отримані розчини, розглядаю осад. Мило практично не утворює піни – вміст солей Кальцію та Магнію високий у всіх зразках.
Дослід №6. Визначення сульфатів
У пробірку вносимо 10 мл досліджуваної води, 0,5 мл соляної кислоти (1: 5) і 2 мл 5% -ного розчину хлориду барію, перемішуємо. За характером осаду що випав, визначаємо орієнтовний вміст сульфатів. Усі зразки №1, 2,3 містять значну кількість сульфатів – спостерігається значне помутніння. (Див.додаток Д)
Проведені дослідження дають змогу зробити висновок, що вода у смт Новгородське з досліджуваних джерел потребує доочищення.
РОЗДІЛ 3. СПОСОБИ ДООЧИЩЕННЯ ВОДИ В ПОБУТІ
Відстоювання
Наливаємо в ємність воду і даємо їй можливість відстоятися близько 8 годин. При цьому ємність кришкою не накриваємо, надавши воді можливість «дихати». Через 4 години з води випаруються майже всі летючі домішки, в тому числі і хлор, яким доблесні комунальні служби наповал убивають гіпотетичні хвороботворні бактерії і мікроби. Ще через 4 години більшість солей важких металів, розчинених у воді, осядуть на дно у вигляді малопомітного осаду.
Завершуємо процедуру відстоювання обережним (без збовтування) зливом 2/3 об’єму відстояної води в інший посуд, а рідину (назвати її водою просто не повертається язик), що залишилася виливаємо геть.
Часткове заморожування
Ємність, наповнену не до країв водою, поміщаємо в морозильну камеру. Під ємність з водою підкладаємо для теплоізоляції шматок пористого картону. Через деякий час на поверхні утворюється невелика крижана кірка. Вона складається з води з домішками важких металів, що замерзає в першу чергу. Видаляємо кірку із посудини і чекаємо, коли замерзне половина решти об’єму води.
Незамерзлу воду зливаємо . В силу своїх хімічних властивостей, замерзає в першу чергу чиста прісна вода, оскільки при кристалізації кристали льоду, що ростуть, витісняють зі свого складу всі сторонні молекули і атоми. Лід, що утворився, розтоплюємо і вживаємо для пиття і приготування їжі.
Насичення води кремнієм
Шматочки купленого в аптеці кремнію ретельно промиваємо, поміщаємо в скляну посудину і заливаємо водою. Розміщуємо в приміщенні з кімнатною температурою і природним освітленням, але так, щоб прямі сонячні промені не потрапляли на ємність з водою. Через 2-3 дні вода буде готова до вживання.
Кремній, будучи дуже сильним активатором води і володіючи бактерицидними властивостями, за час настоювання наситить воду своїми частками на молекулярному рівні, а значить крім очищення додасть такій воді ще й лікувальних властивостей. Насичена кремнієм вода дуже смачна, не містить бактерій і довго зберігається.
Очищення активованим вугіллям
На дно ємності поміщаємо 10 таблеток активованого вугілля, зав’язаних в імпровізований мішечок з марлі чи медичного бинту і заливаємо від 8 до 10 літрів води. Щоб уникнути розмноження різних бактерій і мікроорганізмів ємність з водою слід поставити в прохолодному приміщенні.
Через 8 годин активоване вугілля, що є дуже сильним абсорбентом, поглине більшу частину шкідливих речовин, а вода позбудеться неприємних запахів і значно покращить свій смак.
Очищення води сріблом
У посуд з набраною для очищення водою опускаємо столове срібло або срібні монети. Через 10-12 годин іони срібла, розчинені у воді, очистять її від бактерій. Така «срібна» вода буде зберігатися дуже тривалий час, не втрачаючи своїх смакових якостей. Невеликий мінус – вироби зі срібла після тривалого застосування доведеться чистити.
За бактерицидним впливом срібло значно перевершує хлорку, карболову кислоту й інші сильні дезінфікуючі засоби. Спосіб очищення води сріблом дуже поширений у моряків, підводників і космонавтів.
Кип´ятіння води
Кип’ятіння – найвідоміший і доступний спосіб очищення води. Хоча правильніше було б його називати методом стерилізації, адже кип’ятіння знищує у воді як шкідливі, так і корисні мікроорганізми.
Кип’ятити воду для повного очищення від бактерій і мікроорганізмів необхідно не менше 10 хвилин. Але потрібно знати міру, оскільки в процесі довгого кип’ятіння водопровідної води в ній утворюється такий канцероген, як трихлорметан, і відбувається збільшення концентрації солей важких металів. [2]
ВИСНОВКИ
Приблизно сто років тому централізоване водопостачання та каналізація стали доступними в більшості міст по всьому світу. Вода, яка надходила до споживачів із водопровідного крана, була еталоном чистоти та безпеки. І всі були впевнені в тому, що так буде завжди. Однак пройшли десятиліття і канули в лету ті часи, коли воду з колодязів, неглибоких свердловин і водопровідну воду можна було безбоязно пити без попередньої очистки. Забруднення поверхневих і підземних вод промисловими, побутовими і сільськогосподарськими стоками, а також інфільтратами від звалищ твердих промислових та побутових відходів, зробили свою «чорну» справу. Результат життєдіяльності людства, а нас вже понад 7,2 млрд чоловік, в першу чергу позначився на якості доступних запасів прісної питної води. Недосконалість систем централізованого очищення води у багатьох регіонах і критичний знос водопровідних мереж, посилюють ці проблеми.
Високий рівень забруднення джерел питного водопостачання, недостатня ефективність технології водопідготовки та водопостачання, низький рівень забезпеченості води на душу населення призвели до низької якості питної води в Україні, що стало серйозною загрозою для здоров’я нації. Тому проблема якості питної води була й лишається вкрай актуальною та надзвичайно гострою.
На основі проведених нами досліджень встановлено, що ситуація з якісним станом води у джерелах централізованого водопостачання смт Новгородське за органолептичними та хімічними показниками має нестійкий характер.
Проведені дослідження дають змогу зробити висновок, що вода у смт Новгородське з досліджуваних джерел потребує доочищення. Пропоную наступні способи очищення води в побуті:
- Фільтрування
- Кип’ятіння
- Відстоювання
- Часткове заморожування
- Очищення сріблом
- Очищення активованим вугіллям
- Насичення води кремнієм
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Велика енциклопедія школяра. Оксфорд / Пер. з англ. У. В. Сапціной, А. І. Кіма, Т.В.Сафроновой і др.-М.: ЗАТ “РОСМЕН-ПРЕСС», 2007.
- Г. А. Скоробогатов, А.И. Калинин “Водопроводная вода. Ее химические загрязнения и способы доочистки в домашних условиях” – СПб/издательство С.-Петерб., 2003
- Краузер Б.; Фридмантл М. Химия. Лабораторный практикум.- М:Химия, 1995
- Я познаю мир: Дет. Энцикл.: Экология. / Авт.- сост.А.Е.Чижевский; Худож. В.В.Николаев, А.В. Кардашук, Е.В.Гальдяева. – М.:ООО «Издательство АСТ»: ООО «Издательство Астрель», 2003 .- 410, (6)с.: ил.
- http://korusna.info/pobut/yak-ochystyty-vodu-bez-vykorystannya-filtru-dlya-vody-v-domashnih-umovah.html#ixzz5dMhJO8yW
- https://himanaliz.ua/uk/analiz-vodi-osnovni-pokazniki-rozshif/
- http://ecounit.com.ua/artikle_88.html
- http://medbib.in.ua/gigienicheskie-trebovaniya-normativyi.html
- http://jkg-portal.com.ua/ua/publication/one/pitna-voda-samostjno-ocniti-jakst-45550
ДОДАТКИ
Додаток А
Дослід №1. Визначення кольоровості води
Додаток Б
Дослід №1. Визначення кольоровості води
Додаток В
Дослід №2. Визначення прозорості
Додаток Г
Дослід № 4. Визначення рН-показника
Додаток Д
Дослід №6. Визначення сульфатів

Редакція може не поділяти думку авторів і не несе відповідальність за достовірність інформації. Будь-який передрук матеріалів з сайту може здійснюватись лише при наявності активного гіперпосилання на e-kolosok.org, а також на сам матеріал!






