Підготувала:
Чубай Ольга,
студентка Луцького педагогічного коледжу
Керівник:
Осип Марія Анатоліївна,
викладач біології
Луцького педагогічного коледжу,
фіналістка V Всеукраїнського Інтернет-конкурсу
„УЧИТЕЛЬ РОКУ – 2020” за версією
науково-популярного природничого
журналу „КОЛОСОК” у номінації
„Біологія та основи здоров’я”
ПЕРЕЛІК УМОВНИХ СКОРОЧЕНЬ
ЖК – жирні кислоти
г – грам
мг – міліграм
АДФ – адинозин-5´-дифосфат
АТФ – адинозин-5´-трифосфат
КоА – коезим А
НАДФ – нікотинамідаденіннуклеотид фосфат
КЧ – кислотне число
ЕЧ – естерне число
ЙЧ – йодне число
ПЧ пероксидне число
ЧО число омилення
d204 – густина
n20D – показник кута заломлення
ТШХ– тонкошарова хроматографія
HS-AПБ – ацилпереносний білок
РСЗ – робочий стандартний зразок
БАР – біологічно активні речовини
ВСТУП
Цитрусові рослини містять багато корисних для людського організму речовин та мають чудові смакові якості. Проявляють функціональні властивост, виконують заспокійливу та тонізуючу дію.
Вважається, що на плоди цитрусових на світовому ринку припадає більше третини всіх споживних свіжих фруктів [1].
Актуальність теми: порівняння вмісту біологічно активних речовин в соку цитрусових є важливим для використання цих плодів у різних галузях промисловості (харчовій, фармацевтичній, косметичній).
Мета і завдання дослідження: Дослідити вміст біологічно активних речовин в соку родини цитрусових.
Для досягнення поставленої мети в даній роботі вирішують такі завдання:
- Методом екстракції в апараті Сокслета отримати олії з насіння лимонів, апельсинів, мандаринів та грейпфрутів.
- Дослідити фізико-хімічні параметри (показник заломлення, густину, кислотне число, йодне, пероксидне, ефірне число, число омилення) отриманих олій.
- Дослідити хімічний склад отриманих олій методом ТШХ.
- Провести аналіз жирнокислотного складу отриманих олій, методом газорідинної хроматографії.
- На основі отриманих даних зробити порівняльний аналіз жирних кислот у олії насіння лимонів, апельсинів, мандаринів та грейпфрутів.
Об’єкт дослідження: плоди (лимонів, апельсинів, мандаринів і грейпфрутів).
Предмет дослідження: склад біологічно активних речовин соку лимонів, апельсинів, мандаринів, грейпфрутів, а також порівняти склад біологічно активних речовин в соку цитрусових.
РОЗДІЛ І. ЛІТЕРАТУРНИЙ ОГЛЯД
1.1. Жирні кислоти природних ліпідів
Жирні кислоти є характерними структурними компонентами більшості ліпідів. Це монокарбонові кислоти, що містять від 4 до 24 атомів вуглецю,частіше –12-24. За властивостями вищі жирні кислоти – сполуки, які містять одну гідрофільну карбоксильну групу, що дисоціює у довгий гідрофобний вуглеводневий ланцюг.
Як правило, природні ЖК містять парне число атомів вуглецю. Виділяють насичені, ненасичені ЖК [2].
Ненасичені ЖК мають подвійний зв’язок у цис-положенні, а в поліненасичених подвійні зв’язоки розділені метиленовими групами.
У рослинних оліях переважають жирні кислоти з 18 вуглеводними атомами, їх вміст для більшості рослинних олій становить приблизно 95% від загальної суми жирних кислот.
Таблиця 1.
Мононасичені жирні кислоти
Загальна формула насичених ЖК:CnH2n +1COOH або CH3(CH2) nCOOH
|
Масляна (С4) |
СН3– (СН2)2 СООН |
С3Н7СООН |
|
Лауринова (С12) |
СН3 – (СН2)10 – СООН |
С11Н23СООН |
|
Пальмітинова (С16) |
СН3 – (СН2)14 – СООН |
С15Н31СООН |
|
Стеаринова (С18) |
СН3– (СН2)16 – СООН |
С17Н35СООН |
Таблиця 2.
Мононенасичені жирні кислоти
Загальна формула мононенасичених ЖК:
СН3 – (СН 2)m – CH = CH(CH 2)n – COOH
|
Акрилова (С3) |
СН2 = СН– СООН |
С2Н3СООН |
|
Кротонова (С4) |
СН3–СН = СН–СООН |
С3Н5СООН |
|
Олеїнова (С18) |
СН3 – (СН2)7 – СН = СН – (СН2)7 –СООН |
С17Н33СООН |
Таблиця 3.
Поліненасичені жирні кислоти
Загальна формула полі ненасичених ЖК:
СН 3 – (СН 2) m – (CH = CH(CH 2) х – (СН 2) n– COOH
|
Ліноленова (С18) |
СН3 СН2СН=СН – СН2 СН =СН – СН2 – СН=СН–(СН2)7 СООН |
С17Н29СООН |
|
Лінолева (С18) |
СН3– (СН2)4– СН=СН СН2 СН=СН – (СН2)7– СООН |
С17Н31СООН |
|
Арахідонова (С20) |
СН3 – (СН2)4 – (СН = СН – СН2)4 – (СН2)2– СООН |
С17Н33СООН |
1.2. Родина Цитрусових (Citroideae)
Родина Цитрусових (Citroideae), підродина дводольних квіткових рослин сімейства рутових (Rutaceae). Найбільш надзвичайним в підродині цитрусових і взагалі цілком унікальним, неповторним для інших родин є плід гесперидій, властивий багатьом представникам підродини цитрусових, зокрема для роду цитрус, куди відносяться апельсин, лимон, мандарин, грейпфрут і інші. Гесперидій являє собою дуже своєрідну різновидність ягодоподібного плоду[7].
Лимон (Cіtrus lіmon Burm)
Лимон. Щонайменше 3 тис. років тому люди знали про лимон багато корисного та вживали його з лікувальною метою. Назву рослини тлумачать від малайського слова «лемо», що означає корисний для матерів [7]. Лимони відрізняються від інших цитрусових незначним вмістом цукрів і високою масовою часткою органічних кислот. В плодах лимонів містяться:
Таблиця 4.
Поживні речовини лимону
|
Сухі речовини |
9,6-10,2 |
|
Цукри |
2,0-2,6 |
|
Органічні кислоти |
3,4-8,3 |
|
Білки |
0,3-0,8 |
|
Жири |
0,3-0,8 |
|
Клітковина |
0,4-0,9 |
|
Мінеральні речовини |
0,3-0,5(калію – до 235 мг/100 г, кальцію – 26-27, фосфору – 22-26, заліза – 0,3-0,5 мг/100 г) |
|
Вітаміни |
С–40-85 мг/100 г, p-каротин – 0,4; В1– 0,04; В2 – 0,2; Р – 0,1-0,3 мг/100 г |
У плодах є також інші корисні біологічно активні речовини: флавоноїди (цитронін, гесперидин, діосмин, 7-рамнозид, ери-диктіол); похідні кумарину (лиметин, меранзин, аураптен, біо-кангелицин, бергамоти), а також лимен, кадинен, галактуронова кислота.
У шкірці є також багато корисних речовин, 100г: клітковина — 4,4; цукри— до 6; органічні кислоти— 0,3; пектинові речовини — до 7; мінеральні речовини — до 0,65; ефірні олії — до 0,6 (в складі яких цитраль — 4% надає приємного запаху олії, терпен — 95%, а також — пінен, терпінен, камфен, фелландрен, метилгептенон, дипентен і альдегіди— октиловий, нониловий, каприловий). В шкірці є Р-активні речовини: геспередин, еридиктиол і халкон геспередина. Етерна олія (Oleum Citri) містить переважно лимонен (до 90%), є альдегід (цитраль) (3–5%), терпени (цитроптен), бергамотин; d20D 0,850–0,858; nD20 1,474–1,478; розчиняється у 90% спирті у співвідношенні 1:10 [7,8].
Апельсин (Cіtrus sinensis Osbесk)
Слово «апельсин» німецького походження (від «апфель» – яблуко та «сине» – китайський).
Плід апельсину подібний до плоду лимону в залежності від умов вирощування. М’якість складає біля 3/4 плоду, а решта шкірка і насіння.
В апельсині міститься: цукру – 5 – 6%, вуглеводів – 1,0%, кислот – 2,5%, азотистих речовин – 0,7%, клітковини – 1,0%, води – 90% та золи – 0,5%. Багатий апельсин на вітаміни: А – 0,16- 0,2 мг%, В1 – 0,008 мг%, В2 – 0,08 мг%, С – 66 мг%, а також фосфор – 23 мг%, калій – 197 мг%.
Ефірні олії, що містяться в апельсиновій шкірці, використовують як ароматизатори харчових продуктів. Не обходять його увагою й парфумерна промисловість та косметика. У фармацевтичній промисловості використовують як засіб, що сприяє травленню.
Олія з насіння використовується для виробництва мила [5,8].
Мандарин ( Cіtrus reticulаta Blanco )
Мандарин – це дивовижна рослина, яка завдяки своїм чудовим якостям почала швидко поширюватися спочатку на півдні Франції і в Алжирі, а потім помандрувала до країн Європи.
У ньому міститься близько 40-50 мг% вітаміну С, який зберігається в плодах дуже довго.
Плоди по формі бувають від шароподібного до грушоподібного, з темно-оранжевою шкірочкою, легко відділяється від м’якоті, вона м’ясиста і соковита, легко розділяється на 9-13 дольок. Сік отриманий з м’якоті, оранжевого кольору, кисло-солодкий з приємним ароматом (сахарози 8,56%, органічних кислот 0,88%). Зерна зустрічаються рідко, частіше плоди без зарен. По величині зерна великі і товсті [5,7,8].
Грейпфрут (Citrus paradise Macf)
Плоди круглої форми, діаметром більше як 15 см, шкірка відносно тонка, жовтого кольору або з оранжевим відтінком, м’якуш дуже соковитий, часто рожевого кольору, насіння невелике. В плодах грейпфрута міститься від 34,0 до 48,5 мг вітаміну С на 100 г м’якоті плоду, а також органічні кислоти (0,52,5%), вуглеводів (5-10%).
В червоном’яких плодах крім каротиноїдів, які володіють активністю вітаміну А, містяться і інші речовини з Р-вітамінною активністю. М’якуш містить також білкові речовини, в яких входять життєво необхідні амінокислоти (аланін, аргінін, аспарагін, гісцидин, лізин, серин, цистеїн і інші), а в склад золі входять такі мінеральні речовини, як залізо, калій, натрій, магній, фосфор і сірка. Сік грейпфруту покращує апетит, являється профілактичною і укріплюючою речовиною при інфекційних хворобах [5,7].
1.3. Фізико-хімічні властивості
Рослинні олії за звичайних умов рідкі речовини, маслянисті на дотик, на папері залишають пляму, яка збільшується при нагріванні.
Олії жовтуваті завдяки каротиноїдам або зеленкуваті, якщо присутній хлорофіл.
Запах і смак – специфічні і обумовлені супутніми речовинами.
Олії легко розчинні в органічних розчинниках (діетиловому етері, хлороформі, бензені, гексані, петролейному етері, вазелиновій олії тощо); мало розчинні в етиловому спирті, розчиняються в спирті при нагріванні, але при охолодженні розчин розшаровується; нерозчинні у воді, але в присутності емульгаторів утворюють емульсії.
Жирні олії оптично неактивні, якщо вони не містять залишків оптично активних речовин. Жирні олії мають значну рефракцію: показник заломлення тим вищий, чим більше в жирі гліцеролів з ненасиченими кислотами [9].
Жирнокислотний склад олії міняється в залежності від кліматичних умов [10].
1.4. Основні характеристики олій
Важливими характеристиками олій є такі числові показники як: кислотне, естерне, йодне числа, число омилення та пероксидне число.
Кислотне число (КЧ) – це кількість міліграмів КОН, яка необхідна для нейтралізації вільних ЖК, що містяться в 1 г жиру. Зазвичай олії містять невелику кількість вільних ЖК (1-2%). Однак за тривалого збереження олій вміст цих кислот збільшується. Це знижує їхню харчову якість, тому що вільні ЖК надають олії неприємних запаху і смаку. Багато вільних ЖК міститься також в олії, яку отримують з недозрілого насіння [11].
Естерне число (ЕЧ) називають кількість міліграмів КОН, яка необхідна для омилення естерів, що містяться в 1 г досліджуваної сировини. Естерне число дорівнює різниці між числом омилення та кислотним числом. Величина його залежить від молекулярної маси кислот, що входять до складу жиру: чим вона менша, тим більший показник естерного числа.
Йодне число (ЙЧ) – це кількість грамів йоду, що зв’язується 100 г жиру. Оскільки йод приєднується за місцем подвійного зв’язку, розмір йодного числа характеризує вміст ненасичених кислот в олії [12,13].
Число омилення (ЧО) називають кількість міліграмів калій гідроксиду,яка потрібна для нейтралізації вільних кислот та омилення естерів, що міститься в 1 г досліджуваного жиру. Воно характеризує загальну кількість кислот (вільних і зв’язаних у ацилгліцеридах), що входять до складу жиру.
Пероксидне число (ПЧ) – це об’єм 0,1 н розчину натрій тіосульфату,у мілілітрах витраченого на титрування жиру[13].
РОЗДІЛ ІІ. МЕТОДИ ДОСЛІДЖЕННЯ
2.1. Виділення олії методом екстрагування органічним розчинником
Для екстрагування використовують апарат Сокслета.
Олієвмісне насіння масою 50 г підсушують при температурі 102-105°С від 30 хвилин до 2 годин залежно від вмісту вологи. Потім підсушене насіння ретельно подрібнють. Подрібнене насіння поміщають у екстракційний патрон, який виготовляють із фільтрувального паперу.
Патрон поміщають в екстрактор, який з’єднують із круглодонною колбою та зворотнім холодильником, що має водяне охолодження.
У зібраний апарат Сокслета через холодильник наливають розчин так, щоб патрон був повністю покритий шаром розчинника. Кількість розчинника становить 2/3 об’єму колби.
Колбу апарата встановлюють у гніздо електричної плитки (або водяної) бані. Холодильник заповнюють водою і нагрівають колбу відповідним нагрівачем. Екстрагування олії проводять протягом 3-4 годин при температурі, яка близька до температури кипіння розчинника. Початком екстракції вважається той момент, коли розчинник із насатки екстрактора зіллється у колбу вдруге.
Після цього екстракцію проводять неперервно.
Після закінчення екстракції перестають нагрівати колбу, дають вистигнути, виключають воду і знімають холодильник.
Розчинник відганяють за допомогою приладу для прямої перегонки. Залишки розчинника упарюють за допомогою водострумного насоса. Пробу відфільтровують на скляному фільтрі з приєднаним водострумним насосом. Колба з олією зважують і за різницею мас порожньої колби і колби з олією знаходять масу та вираховують вихід олії у перерахунку на 100 г сухого насіння. Перше зважування проводять після охолодження в екстракторі протягом 40-60 хв.
Масову частку олії в очищеному від домішок, подрібненому і підсушеному насінні розраховують за формулою:
Mc = (m-m1)/m2,
де m – маса колби з олією, г;
m1 – маса пустої колби, г;
(m-m1) – кількість олії, г;
m2 – наважка подрібненого насіння [10].
2.2. Дослідження жирнокислотного складу рослинних олій методом газової хроматографії
Робота проводиться з різними оліями рослиного походження.
Приготування розчину натрій метилату
Зважують1,15 металічного натрію в стакані для зважування. Результат записують у грамах до другого знаку.
В міру колбу ємністю 25 см3 наливають 10-12 см3 метанолу, до нього додають маленькими шматочками металічний натрій. Після розчинення розчин охолоджують до кімнатної температури та доводять метанолом до мітки. Зберігають розчин у холодильнику .
Приготування метилових естерів жирних кислот
Пробу досліджуваного жиру добре перемішують. У скляну пробірку відбирають піпеткою 2 краплі жиру (зважити, у всіх дослідах використовувати однакову кількість проби), розчиняють їх у 1,9 мл гексану.
У розчин вводять 0,1 мл розчину натрій метилату в метанолі концентрацією 2 моль/л. Після інтенсивного перемішування протягом 2 хвилин реакційну суміш відстоюють 5 хвилин та фільтрують через паперовий фільтр. Розчин готовий до аналізу. Готовий розчин зберігають у холодильнику не більше 2 діб.
Підготовка хроматографа до роботи
Підключення хроматографа, підготовка та встановлення колонок, вивід приладу на робочий режим здійснюється згідно інструкцій по встановленню та налаштуванню хроматографа.
Проведення вимірювання
На хроматографі встановлюють наступні умови аналізу масел, що не містять низькомолекулярних кислот ( крім кокосового ):
Температура термостату колонок 160-240°С;
Температура випаровувача – 220°С;
Температура дитектора – 250°С;
Швидкість потоку газу-носія (азот) – 30-40мл/хв;
Об’єм проби біля 1 мкл розчину метилових естерів у гексані [18].
2.3. Розділення загальної фракції ліпідів методом тонкошарової хроматографії
Тонкошарова хроматографія – це ефективний, переважно аналітичний метод швидкого розділення низькомолекулярних речовин: ліпідів, амінокислот, нуклеотидів, вітамінів та інших. Досліджуваний зразок наносять на тонкий шар силікагелю, закріпленого на пластинці з фольги або скла. Пластинку поміщають у хроматографічну камеру з невеликою кількістю розчинника. Фронт розчинника піднімається по пластинці під дією капілярних сил, захоплюючи речовини,що містятьсяу пробі. Швидкість просування речовин, що аналізуються, залежить від їх розподілу між нерухомою (гідрофітний силікагель) і рухомою (неполярний розчинник) фазами та розчинності в останній. Хроматографічний процес закінчують у той момент, коли розчинник досягає верхнього краю пластинки. Пластинку із силікагелем висушують, а досліджувані речовини виявляють за допомогою відповідних барвників. Для кожної речовини розділеного зразка розраховують величину Rf. Отримані значення Rf порівнюють зі значеннями Rf контрольних речовин (свідків) та ідентифікують сполуки, що є присутні у зразку.
Приготування пластинок. Пластинки закріпленого шару силікагелю готують заздалегідь у такий спосіб.
Скляні пластинки (краще фотопластинки) розміром 17,5×13 см ретельно миють їхромовою сумішшю й обполікують багато разів водопровідною водою, потім 3-5 разів дистильованою, витирають чистою марлею, протирають етиловим спиртом і зберігають у чистому поліетиленовому пакеті в окремій коробці.
Нерухомою фазою при поділі служить силікагель КСК, для закріплення силікагелю використовують хімічно чистий гіпс – CаSO4.
Для приготування сорбційнної маси 6 г силікагелю і 0,35 г гіпсу енергійно струшують 3-5 хвилин у колбі (можна з гумовою пробкою, захищеною плівкою). Суміш висипають у ступку, поступово, при ретельному розтиранні, невеликими порціями по 3-5 мл додають дистильовану воду – всього 15-17 мл. Змішування силікагелю і гіпсу з водою закінчують протягом 1,5-2 хвилин (стежити за секундоміром).
Отримана маса повинна бути однорідною і без пухирців повітря.
Готову суміш тонким безперервним струменем виливають у центр пластинки і погойдуванням пластинки розпроділяють її рівним шаром по всій поверхні. Пластинку сушать при кімнатній температурі 24 години на столику з рівнем, а потім активують у сушильній шафі при 105 °кщо пластинки не використовують відразу, їх зберігають у ексикаторі над СаСl2 .
Підготовка хроматографічної камери. Розгонку загальної фракції ліпідів проводять сумішшю розчинників гексан-діетиловий етер-льодяна оцтова кислота у співвідношенні 78:25:2 або гексан-діетиловий етер-мурашина кислота у співвідношенні 80:80:2 у будь-якій герметично закритій посудині з плоским дном. Стінки камери для кращого насичення вистилають фільтрувальним папером і в камеру наливають суміш розчинників. Щільно закриту камеру залишають на 2-3 години для насичення парами розчинника. Під час аналізу стежте, щоб пластинка не торкалась змоченого паперу, бо розчинник буде перетікати на пластинку.
Нанесення екстракту на пластинку. Ліпіди, виділені з тканин, розчиняють у 1 мл хлороформу. Хлороформний екстракт ліпідів наносять на пластинку за допомогою мікропіпетки. Лінія старту повинна бути на відстані 1,5см від нижнього краю пластинки, відстань між крапками нанесення 1-2см (не менш). Розчин наносять дуже маленькими краплями, не доторкаючись піпеткою до пластинки, або в одну крапку, або вузькою горизонтальною смужкою (8мм), крапля до краплі. Загальний обсяг екстракту, що наносять на пластинку, – 0,05-0,1 мл.
На цю ж пластинку наносять свідки: 1 % хлороформні розчини холестеролу, фосфатидилетаноламіну і триацилгліцеролів (свиняче сало) у кількості 0,04-0,05 мл. Величина Rf залежить від кількості нанесеної на пластинку речовини, (кращий результат досягається при нанесенні на пластинку 0,5-1,0 мг проби). У разі потреби розділення великих кількостей речовин можна використовувати препаративне розділення ліпідів методом тонкошарової хроматографії. Цим способом можна розділити суміші речовин порядку 50 мг і більше.
Розділення і проявлення. Після нанесення ліпідів пластинку поміщають у камеру, занурюючи її у розчинник на 5 мм. Камеру герметично закривають. Розгонка продовжується 50-60 хвилин при кімнатній температурі. Підйом рідини не повинний бути вище 10-12 см, тому що при великому підйомі відбувається дифузія плям і спостерігається коливання величини Rf. Після розгонки пластинку висушують на повітрі протягом 30 хвилин. Хроматограму проявляють, обережно обприскуючи зі скляного пульверизатора 10 % спиртовим розчоном фосфомолібденової кислоти, і потім, через 1-2 хвилин витримують її у сушильній шафі при температурі 80-100 °С до появи на жовтому тлі синіх плям ліпідів. Надлишок проявника може привести до занадто сильного забарвлення пластинки.
Розташування ліпідів на хроматограмі наступне: чітко виявляються 7-8 плям. У першій плямі на старті знаходяться фосфогліцерини, вище – не ідентифіковані сполуки, у третій плямі міститься холестерол, потім моно-, ди-, триацилгліцероли відповідно, в останній плямі – естери холестеролу. Між ди- і триацилгліцероли розташовуються вільні жирні кислоти, але вони не виявляються фосфомолібденовою кислотою (проявники вільних жирних кислот: родамін або 0,2% спиртової розчин 2,6-дихлорфлуоресцина в ультрафіолеті). Замість фосфомолібденової кислоти можна використовувати спосіб прояву ліпідів у парах йоду. В останньому випадку виявляються всі ліпіди. Для цього суху пластинку поміщають на кілька хвилин у закриту посудину (можна ексикатор), наповнений кристалами йоду (під витяжкою!)[19].
2.4. Визначення фізико-хімічних показників олії
Фізико-хімічні показники виділених з олій цитрусових визначаємо за такими методиками [17,19,20,21].
2.4.1 Визначення показника заломлення олії
Визначення показника заломлення олії проводять на рефрактометрі ИРФ-454Б.
На призму рефрактометра наносять краплю олії за допомогою скляної палички, не торкаючись до полірованої поверхні. Закривши призму, встановлюють чіткість зображення та оптимальне освітлення. Вимірюють показник заломлення олії при кімнатній температурі. При зміні результатів, одержують приведене значення показника заломлення при температурі 20°С.
2.4.2. Визначення густини олії
Величина густини залежить від температури. Відносну густину зазвичай визначають за водою, густина якої при 4°С майже дорівнює одиниці (0,99997г/см3).
Визначення густини проводять у пікнометрів ємності 1– 2 мл. Чистий та сухий пікнометр зважують на аналітичних вагах при кімнатній температурі. Потім визначають «водне число пікнометра», що є постійним для кожного пікнометра і відповідає масі води в об’ємі пікнометра при 20°С, приведеної до маси води при 4°С,
mH2O(20°C)/ mH2O(4°C)=0,99823/1
x(mH2O(4°C))= mH2O(20°C)/0,99823,
де 0,99823 г/см3 густина води при 20°С.
Отримана величина m Н2О (4°С) є «водним числом» або «водною константою» пікнометра.
Для визначення густини досліджуваної рідини зважують сухий, чистий пікнометр і порівнюють його масу з масою, визначеною при визначенні «водної константи».
Потім пікнометр заповнюють досліджуваною рідиною та проводять аналогічні вимірювання, як для води.
Відношення маси речовини в об’ємі даного пікнометра до величини «водної константи» відповідає густині даної речовини:
d420 =m-mn /B (2.1.)
В – «водна константа» пікнометра;
М – маса пікнометра з досліджуваною речовиною;
mn – маса пікнометра порожнього.
За результат аналізу приймають середнє арефмитичне трьох паралельних визначень.
2.4.3. Визначення кислотного числа олії
Хід роботи. До 1 г олії додають 5 мг спирту нейтралізованого за фенолфталеїном, добре перемішують до максимального розчинення вільних жирних кислот і титрують розчином КОН до появи рожевого забарвлення (забарвлення не повинно зникати протягом 0,5 – 1 хв).
Кількість КОН у міліграмах, витрачену на титрування вільних жирових кислот, що містяться в 1 г жиру, визначають за формолою:
КЧ=АQ/а (2.2.)
де А – об’єм розчину КОН (0,1 моль/л), витрачений на титрування досліджуваної проби мл;
А – наважка жиру, г;
Q – кількість КОН (5,61мл), еквівалентна 1 мл розчину КОН (0,1 моль/л).
2.4.4. Визначення йодного числа олії
Хід роботи. В одну колбу (досліджувана проба) вносять наважку 0,1-0,2 г, у другу, (контрольна проба) – 0,1-0,2 мл води по 10 мл спиртового розчину йоду, перемішують заливають на 10 хвилин. Далі вміст колб титрують розчином Na2S2O3 до появи жовтого забарвлення. Потім, додавши 1 мг розчину крохмалю, суміш титрують до зникнення синього запарвлення. Йодне число визначають за формолою:
ЙЧ=(В-А)fQ1000/a1000 (2.3.)
де (В-А) – різниця результатів титруваня контрольного досліджуваного зразків у розчині гіпосульфіду (0,05моль/л), мл;
а – наважка розчину жиру, г;
f – коефіцієнт поправки на титр розчину Na2S2O3 (0,05моль/л);
Q – кількість І2 (12,69 мг), еквівалент 1 мл розчину Na2S2O3 (0,05моль/л).
2.4.5. Визначення пероксидного числа олії
Пероксидне чиcло – це об’єм 0,1 н розчину натрій тіосульфату,у мілілітрах витраченого на титрування жиру.
Хід виконання: У конічну колбу зі шліфом на 200 мл поміщали 5 г жиру (з точністю до сотих) олійного екстракту, додали 10 мл хлороформу, інтенсивно перемішували, додоли 15 мл ацетатної кислоти та 1 мл розчину калій йодиду.
Колбу закрили корком і інтенсивно струшували протягом 1 хв і ставили на 5 хвилин у тепле місце. Потім додали 75 мл води та 2-3 краплі крохмалю, розчин набуває синього кольору. Титрування проводили 0,002 н розчином натрій тіосульфату до знебарвлення забарвлення.
Розрахунок проводять за формуло:
П.Ч.=((V1-V0)*1000/m)*C (2.4.)
V0 – об’єм розчину тіосульфату натрію, використаний на контрольний дослід, см3.
V1 – об’єм розчину тіосульфату натрію, використовують для вимірювання, см3.
С – концентрація використаного розчину тіосульфату натрію, моль/дм3.
m – маса досліджуваної проби, в г.
1000 – коефіцієнт перерахунку результату ммоль/кг.
2.4.6. Визначення числа омилення
Хід роботи. В одну колбу (досліджувану пробу) поміщають 0,5 г жиру, в другу (контрольну пробу) – 0,5 мл води. В обидві колби доливають по 15 мл спиртового розчину КОН і кип’ятять із зворотнім холодильником на водяній бані протягом 50 хв до повного омилення гліцеридів і нейтралізації вільних жирних кислот. Потім у обидві колби додають по десять краплин розчину фенолфталеїну та титрують розчином НСІ до зникнення рожевого забарвлення (до нейтральної реакції).
Кількість КОН у мг, витрачена на нейтралізацію всіх жирних кислот, що містяться 1 г жиру, визначають за формолою:
ЧО=(В-А) fQ/a, (2.5.)
(В-А) – різниця результатів титрування контрольного та досліджуваного зразків розчином соляної кислоти (0,5 моль/л),мл;
а – наважка досліджуваного жиру, г;
Q – кількість КОН (28 мг), яка еквівалентна 1мл розчину КОН (0,5 моль/л).
РОЗДІЛ IІІ. ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА
3.1. Виділення дослідних олій з насіння цитрусових
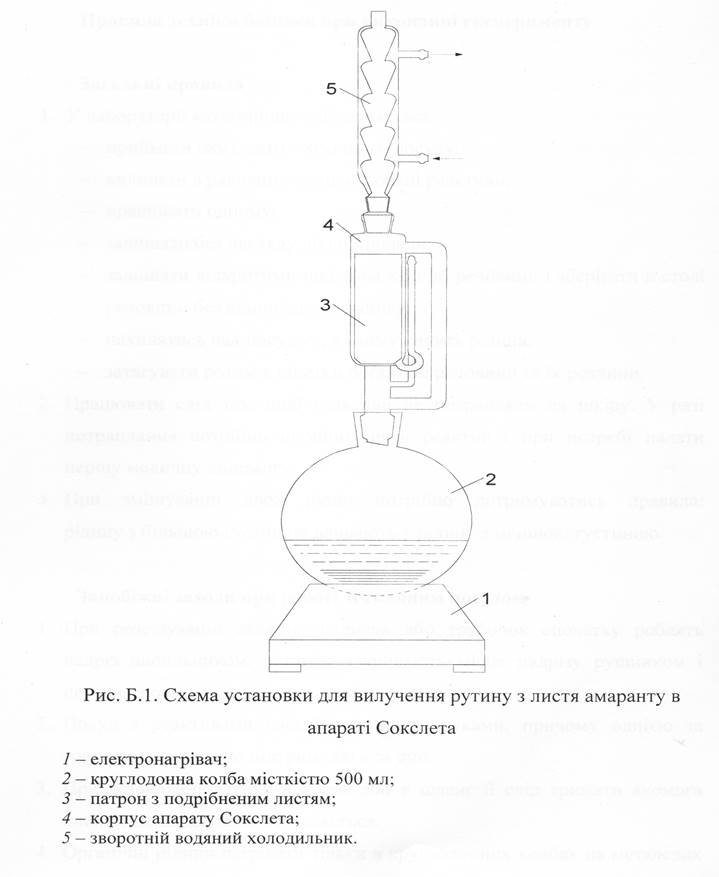
Досліджувані олії отримували методом вичерпної екстракції н-гексаном у апараті Сокслета (додаток В).
Як сировину використовували насіння лимонів, апельсинів, мандаринів, грейпфрутів.
Для одержання олій насіння з цитрусових (лимону, апельсину, мандарину та грейпфруту) попередньо висушували на повітрі. Після цього за допомогою млинка «Мрія» насіння подрібнили, попередньо взявши такі наважки: Лимону – 47,10 г, апельсину – 52,16 г, мандарину – 75,40 г, грейпфруту – 19,3 г.
Як розчинник використовували н-гексан (приблизно 2/3 колби). Екстракцію проводили 2,5 – 3 години. Після припинення екстракції кола з розчином потрібно охолодити і після цього здійснювати відгін н-гексану методом простої перегонки. Гексан опарювали за допомогою водяного охолодження (водяний холодильник). Виділення н-гексану відбувалося за температури 67-68°С (температура кипіння гексану). Вихід отриманих олій з насіння цитрусових становить:
Масова частка з насіння лимонів Мс=66%
Масова частка з насіння апельсинів Мс=52%
Масова частка з насіння мандаринів Мс=34%
Масова частка з насіння грейпфрутів Мс=25%
Маса олії з насінням лимонів m=33 г
Маса олії з насінням апельсинів m=26 г
Маса олії з насінням мандаринів m=17 г
Маса олії з насінням грейпфрутів m=12,5 г
3.2. Дослідження жирокислотного складу олій з насіння лимонів, апельсинів, мандаринів, грейфрутів
3.2.1. Хроматографічне визначення
Підготовленні проби рослинних олій досліджували на газовому хроматографі.
Якісний і кількісний склад олії з насіння лимонів, апельсинів, мандаринів, грейпфрутів методом газорідинної хроматографії.
У скляну пробірку відбирають піпеткою 2 краплі жиру (зважити, у всіх дослідах використовувати однакову кількість проби), розчиняють їх у 1,9 мл гексану. Пробу розчину метилових естерів жирних кислот у гексані розділяли на газовому аналітичному лабораторному хроматографі “Кристалл 2000М”.
У розчин вводять 0,1 мл розчинника метилату натрію в метанолі. Після інтенсивного перемішування протягом 2 хвилин реакційну суміш відстоюють 5 хвилин та фільтрують через паперовий фільтр. Розчин готовий до аналізу. Умови проведення аналізу: температура термостату колонок 160-240°С, температура випаровувала – 220°С, температура дитектора – 250°С, швидкість потоку газу-носія (азот) – 30-40мл/хв. Об’єм проби біля 1 мкл розчину метилових естерів у гексані.
Для градуювання колонки використовували набір стандартів метилових естерів жирних кислот в індивідуальних упаковках. Ідентифікацію ЖК кислот проводили використовуючи величини часу утримання (tR) метилових естерів жирних кислот.
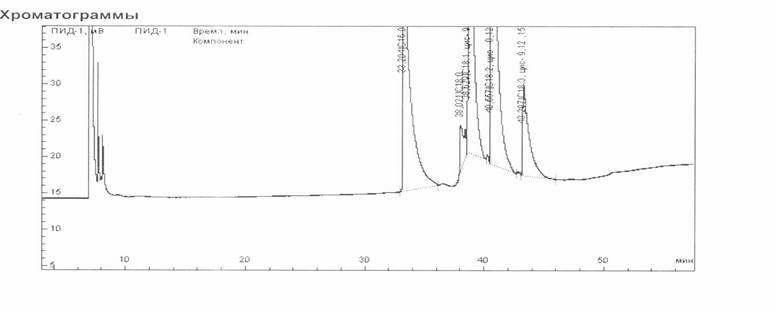
Таблиця 5.1.
Розрахунок за компонентами складу олії з насіння лимону
|
№ |
Час, хв |
Компонент |
Група |
Лін. індекс |
Лог. індекс |
Висота |
Вміст, % |
Детектор |
|
1 |
33,204 |
С16:0 |
33,298 |
23,971 |
ПИД-1 |
|||
|
2 |
38,021 |
С18:0 |
6,731 |
2,834 |
ПИД-1 |
|||
|
3 |
38,629 |
С18:1, цис-9 |
цис- олеїнова |
91,940 |
28,992 |
ПИД-1 |
||
|
4 |
40,557 |
С18:2, цис-9,12,15 |
110,253 |
36,444 |
ПИД-1 |
|||
|
5 |
43,297 |
С18:3, цис-9,12,15 |
12,659 |
7,759 |
ПИД-1 |
Узагальнена хроматографія подана на рисунку 4.1
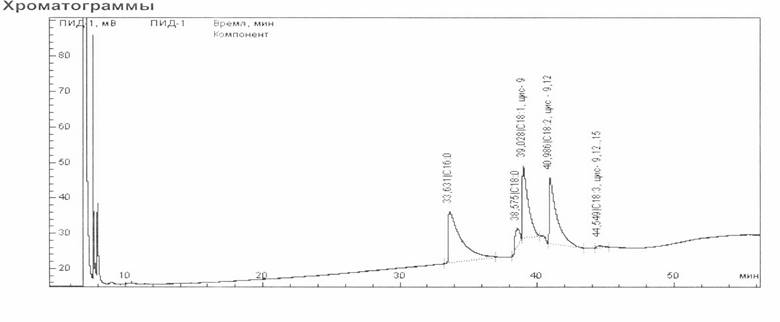
Таблиця 5.2.
Розрахунок за компонентами складу олії з насіння апельсину
|
№ |
Час, хв |
Компонент |
Група |
Лін. індекс |
Лог. індекс |
Висота |
Вміст, % |
Детектор |
|
1 |
33,631 |
С16:0 |
14,672 |
39,907 |
ПИД-1 |
|||
|
2 |
38,575 |
С18:0 |
5,300 |
5,024 |
ПИД-1 |
|||
|
3 |
39,028 |
С18:1, цис-9 |
цис- олеїнова |
20,546 |
24,238 |
ПИД-1 |
||
|
4 |
40,986 |
С18:2, цис-9,12 |
18,711 |
29,880 |
ПИД-1 |
|||
|
5 |
44,549 |
С18:3, цис-9,12,15 |
0,634 |
0,952 |
ПИД-1 |
Узагальнена хроматограма подана на рис. 4.2.
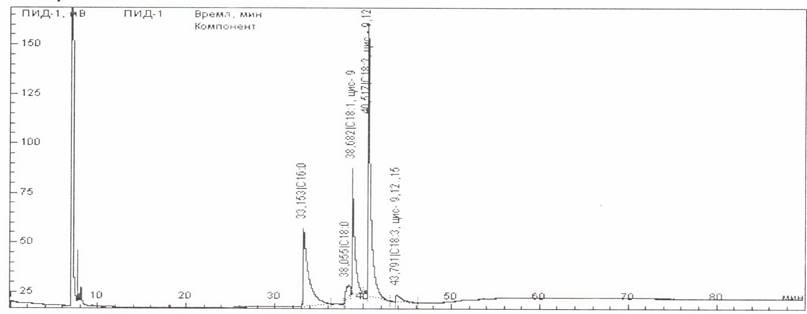
Таблиця 5.3.
Розрахунок за компонентами складу олії з насіння мандарину
|
№ |
Час, хв |
Компонент |
Група |
Лін. індекс |
Лог. індекс |
Висота |
Вміст, % |
Детектор |
|
1 |
33,153 |
С16:0 |
39,486 |
28,767 |
ПИД-1 |
|||
|
2 |
38,055 |
С18:0 |
7,050 |
3,381 |
ПИД-1 |
|||
|
3 |
38,682 |
С18:1, цис-9 |
цисолеїнова |
63,835 |
21,986 |
ПИД-1 |
||
|
4 |
40,517 |
С18:2, цис-9,12 |
138,441 |
43,168 |
ПИД-1 |
|||
|
5 |
43,791 |
С18:3, цис-9,12,15 |
3,525 |
2,698 |
ПИД-1 |
Узагальнена хроматограма подана на рисунку 4.3.
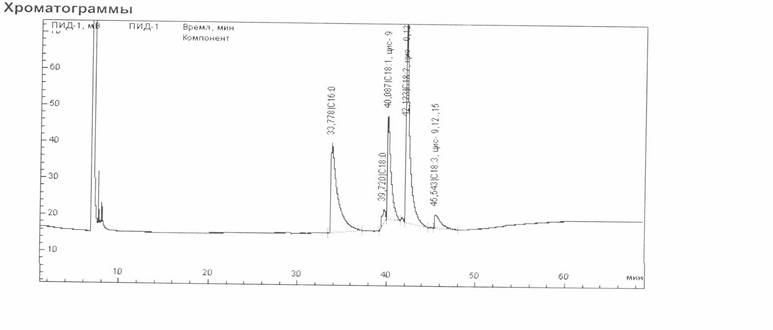
Таблиця 5.4.
Розрахунок за компонентами складу олії з насіння грейпфруту
|
№ |
Час, хв |
Компонент |
Група |
Лін. індекс |
Лог. індекс |
Висота |
Вміст% |
Детектор |
|
1 |
33,778 |
С16:0 |
24,490 |
32,315 |
ПИД-1 |
|||
|
2 |
39,720 |
С18:0 |
3,703 |
2,393 |
ПИД-1 |
|||
|
3 |
40,087 |
С18:1, цис-9 |
Цис-олеїнова |
28,311 |
19,621 |
ПИД-1 |
||
|
4 |
42,123 |
С18:2, цис-9,12 |
58,331 |
41,109 |
ПИД-1 |
|||
|
5 |
45,543 |
С18:3, цис-9,12,15 |
3,730 |
4,562 |
ПИД-1 |
Узагальнена хроматограма подана на рисунку 4.4.
3.3. Визначення фізико-хімічних показників олії
3.3.1. Визначення густини олії
Визначення густани проводили за допомогою пікнометра. Пікнометр брали об’ємом 10 мл, спочатку визначили масу пустого після цього з водою, а тоді з
досліджуваною олією. За отриманими даними визначили густину олії з насіння цитрусових і отримали наступні дані:
Густина олії з насіння лимонів d420=0,5515 г/см3 ;
Густина олії з насіння апельсинів d420=0,5114 г/см3 ;
Густина олії з насіння мандаринів d420=0,5144 г/см3 ;
Густина олії з насіння грейпфрутів d420=0,5884 г/см3 .
3.3.2. Визначення показника заломлення олії
Визначення показника заломлення олії проводили на рефрактометрі ИРФ
454Б.
Показник заломлення олії з насіння лимонів nD20=1,4624;
Показник заломлення олії з насіння апельсинів nD20=1,4547;
Показник заломлення олії з насіння мандаринів nD20=1,4635;
Показник заломлення олії з насіння грейпфрутів nD20=1,4605.
3.3.3. Визначення числа омилення олії
Для визначення числа омилення ми використовували досліджувану олію та спиртовий розчин КОН, кип’ятили на водяній бані зі зворотнім холодильником протягом 50 хвилин до повного омилення гліцеролів. Після охолодження розчину додали фенолфталеїн та титрували НСl до зникнення рожевого забарвлення.
Таблиця 6.1.
Дані обрахунку ЧО
|
Досліджувана олія |
Кількість НСl V1, (мл) |
Кількість НСl V2, (мл) |
ЧО |
|
Лимонна |
18 |
16,5 |
84 |
|
Апельсинова |
14 |
11,5 |
140 |
|
Мандаринова |
15 |
13 |
112 |
|
Грейпфрутова |
19,5 |
16 |
196 |
3.3.4. Визначення кислотного числа олії
За кислотним числом визначали кількість вільних кислот. Для проведення експерименту брали досліджувану олій та спирт нейтралізований за фенолфталеїном, добре перемішали та титрували розчином КОН до появи рожевого забарвлення.
Таблиця 6.2.
Дані обрахунку КЧ
|
Досліджувана олія |
Кількість КОН V, (мл) |
КЧ |
|
Лимонна |
0,1 |
0,562 |
|
Апельсинова |
0,3 |
1,683 |
|
Мандаринова |
0,1 |
0,562 |
|
Грейпфрутова |
0,6 |
3,336 |
3.3.5. Визначення естерного числа олії
Естерне число визначали за різницею між ЧО олії та її КЧ.
Таблиця 6.3.
Дані обрахунку ЕЧ
|
Досліджена олія |
ЧО |
КЧ |
ЕЧ |
|
Лимонна |
84 |
0,562 |
83,438 |
|
Апельсинова |
140 |
1,683 |
138,317 |
|
Мандаринова |
112 |
0,562 |
111,438 |
|
Грейпфрутова |
196 |
3,366 |
192,634 |
3.3.6. Визначення йодного числа олії
Визначення йодного числа проводили за методикою: до досліджуваної олії додавали спиртовий розчин йоду перемішували і залишали на 10 хвилин. Тоді вміст колби титрували розчином Na2S2O3 до появи жовтого забарвлення. Потім, додавши розчин крохмалю, суміш титрують до зникнення синього запарвлення.
Таблиця 6.4.
Дані обрахунку ЙЧ
|
Досліджена олія |
Кількість Na2S2O3, мл (контр.) |
Кількість Na2S2O3, мл (досл.) |
ЙЧ |
|
Лимонна |
11,9 |
9,7 |
25,38 |
|
Апельсинова |
12 |
10,5 |
38,07 |
|
Мандаринова |
8,9 |
8,3 |
15,23 |
|
Грейпфрутова |
23 |
22 |
55,84 |
3.3.7. Визначення пероксидного числа олії
Для проведення експерименту у конічну колбу зі шліфом поміщали досліджувану олію, додавали хлороформ, інтенсивно перемішували, додавали ацетатну кислоту та розчин КІ. Колбу закрили корком, інтенсивно струшували протягом 1 хвилини і ставили на 5 хвилин у темне місце. Після цього додали 75 мл води та 2 3 краплі крохмалю, розчин набував синього кольору. Титрування проводили 0,002 н розчином Na2S2O3 до знебарвлення розчину.
Таблиця 6.5.
Дані обрахунку ПЧ
|
Досліджена олія |
Кількість Na2S2O3, мл (контр.) |
Кількість Na2S2O3, мл (досл.) |
ПЧ |
|
Лимонна |
36 |
31 |
100 |
|
Апельсинова |
26 |
23 |
60 |
|
Мандаринова |
45 |
41 |
80 |
|
Грейпфрутова |
19 |
17 |
40 |
РОЗДІЛ ІV. РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ
4.1. Визначення фізико-хімічних характеристик олії лимонів, апельсинів, мандаринів, грейпфрутів
Екстракцією насіння лимонів, апельсинів, мандаринів, грейпфрутів н-гексаном виділено олії, які є відповідно жовтого та коричнево-жовтого кольору.
Провели хімічне дослідження олії: визначили хімічні числові показники, а також встановили фізичні (густина, показник заломлення) числові показники.
В таблиці наведені основні хімічні характеристики олій, розраховані за результатами досліджень.
Таблиця 11.1.
Зведені дані фізико-хімічних показників олії виділеної з насіння лимонів, апельсинів,мандаринів, грейпфрутів
|
Показник |
Насіння линонів |
Насіння апельсинів |
Насіння мандаринів |
Насіння грейпфрутів |
|
Показник заломлення |
1,4624 |
1,4547 |
1,4635 |
1,4605 |
|
Число омилення, мг КОН |
84 |
140 |
112 |
196 |
|
Кислотне число, мг КОН |
0,562 |
1,683 |
0,562 |
3,366 |
|
Естерне число, мг КОН |
83,438 |
138,317 |
111,438 |
192,634 |
|
Йодне число, % йоду |
25,38 |
38,07 |
15,23 |
55,84 |
|
Пероксидне число, мл Na2S2O3 |
100 |
60 |
80 |
40 |
4.2. Визначення усередненого вмісту ω6/ω3 ненасичених жирних кислот у досліджуваних оліях насіння цитрусових
Олія насіння лимону
Експериментально (з хроматограми):
С18:1 ω6 28,992 С18:2 ω6 36,444 С18:3 ω3 7,759
Співвідношення ω6/ω3 відповідно становить:
ω6/ω3= 28,992+36,444/7,759=8:1
Олія насіння апельсину
Експериментально (з хроматограми):
С18:1 ω6 24,238 С18:2 ω6 29,880 С18:3 ω3 0,952
Співвідношення ω6/ω3 відповідно становить:
ω6/ω3= 24,238+29,880/0,952=57:1
Отримане співвідношення ω6/ω3 не входить в межі літературних значень.
Олія насіння мандарину
Експериментально (з хроматограми):
С18:1 ω6 21,986 С18:2 ω6 138,441 С18:3 ω3 3,525
Співвідношення ω6/ω3 відповідно становить:
ω6/ω3= 21,986+138,441/3,525=46:1
Олія насіння грейпфруту
Експериментально (з хроматограми):
С18:1 ω6 19,621 С18:2 ω6 41,109 С18:3 ω3 4,562
Співвідношення ω6/ω3 відповідно становить:
ω6/ω3= 19,621+41,109/4,562=13:1
В результаті нашого дослідження було виявлено, що всі досліджувані нами рослинні олії з насіння лимонів, апельсинів, мандаринів, грейпфрутів містять різний спектр жирних кислот. У олії насіння лимонів міститься найбільше лінолевої кислоти (36,4%), значно менше олеїнової кислоти (29,0%), на третьому місці пальмітинова кислота (24,0%), далі ліноленова (7,8%), стеаринова (2,8%) кислоти. У апельсиновій олії найбільший вміст пальмітинової кислоти (40,0%), менше лінолевої кислоти (29,9%), олеїнової кислоти (24,2%), стеаринової кислоти (5,0%), ліноленової кислоти (1,0%). Олія насіння мандаринів найбільше містить лінолевої кислоти (42,4%), значно менше пальмітинової кислоти (28,8%), олеїнової кислоти (22,0%), ліноленової кислоти (3,5%) і найменше стеаринової кислоти (3,4%). У олії насіння грейпфрутів в більшій мірі міститься лінолевої кислоти (41,1%) на другому місці пальмітинова кислота (32,3%), олеїнової кислоти міститься (19,6%), ліноленової кислоти (4,6%), стеаринової кислоти (2,4%).
Як видно з результатів дослідження вміст та співвідношення жирних кислот у оліях насіння цитрусових є дуже схожі, що може свідчити про генетичне походження цих рослин від спільного предка.
Співвідношення ω6/ω3 для олії з насіння цитрусових (лимону, апельсину, мандарину, грейпфруту) становить: лимону 8,4%, апельсину 56,8%, мандарину 24,1%, мандарину 13,3%.
4.3. Визначення жирнокислотного складу олій методом газорідинної хроматографії
Таблиця 11.2.
Жирнокислотний склад рослинних олій (%)
|
Жирні кислоти/Олія |
Олія з насіння лимонів |
Олія з насіння апельсинів |
Олія з насіння мандаринів |
Олія з насіння грейпфрутів |
|
Пальмітинова С16:0 |
24,0 |
39,9 |
28,8 |
32,3 |
|
Стеаринова С18:0 |
2,8 |
5,0 |
3,4 |
2,4 |
|
Олеїнова С18:1 |
29,0 |
24,2 |
22,0 |
19,6 |
|
Лінолева С18:2 |
36,4 |
29,9 |
43,2 |
41,1 |
|
Ліноленова С18:3 |
7,8 |
1,0 |
2,7 |
4,6 |
|
Насичені |
26,8 |
44,9 |
32,148 |
34,7 |
|
Мононенасичені |
65,4 |
54,1 |
65,2 |
60,7 |
|
Поліненасичені |
7,8 |
1,0 |
2,7 |
4,6 |
|
ω6/ω3 |
8,4 |
56,8 |
24,1 |
13,3 |
Висновки
- Методом вичерпної екстракції гексаном отримали олії з насіння лимонів, апельсинів, мандаринів, грейпфрутів. Вихід олій становить відповідно: лимонів – 66%, апельсинів – 52%, мандаринів – 34%, грейпфрутів – 25%.
- Методом газорідинної хроматографії встановлено, що олія з насіння лимонів містить пальмітинову (24,0%), стеаринову (2,8%), олеїнову – (29,0%), лінолеву – (36,4%), ліноленову – (7,8%) кислоти. Олія насіння апельсинів містить пальмітинову – (40,0%), стеаринову – (5,0%), олеїнову – (24,2%), лінолеву – (30,0%), ліноленову – (1,0%) кислоти. Олія насіння мандаринів містить пальмітинову – (28,8%), стеаринову – (3,4%), олеїнову – (22,0%), лінолеву – (43,2%), ліноленової кислоти – (3,5%). Олія насіння грейпфрутів містить пальмітинову – (32,3%), стеаринову – (2,4%), олеїнову – (19,6%), лінолеву – (41,1%), ліноленову – (4,6%) кислоти.
- Встановлено, що вміст та співвідношення жирних кислот досліджуваних олій роду Цитрусових є дуже схожими, що може свідчити про їх спільне походження (сімейство Рутових родина Цитрусові).
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Біологія: Навч. посібник / [Слюсарів А.О., Самсонов О. В.,Мухін В.М. та ін..]; за ред.. та пер. з рос. Мотузеного В. О. 2-е вид. К.: Вищ.шк.,1995.607с.
- Гонський Я.І., Максимчук Г.П.,Калиновський М.І. Біохімія людини: Підручник.Тернопіль: Укрмедкнига, 2002744с.
- Химическая энциклопедия. В5m. М., 1990; Губський Ю. І.:4
- НосенкоТ.Т., Пешук Л.В.. Біохімія та технологія оліє жирової сировини. К.:Центр учб. літ.Міністерство освіти і науки України,2011.207с.
- Даныкин В.В. Цитрусовый сад в комнате 3е изд. М.:Агропрому,1991.
- Кучерява Л.Ф. Система вищих рослин К.: Фітосоціоцентр, 1997-355с.
- Квіти України. Види цитрусових та їх характеристика, 2001-№12
- Карпович В.Н. Фармакогнезия / Карпович В.Н., Безпалова Е.И. М.: Медицина, 1977. 64с.
- Биологический енциклопедический словар.М.: Большая российская энциклопедия,1995.634с.
- Шарп Дж., Практикум по органической химии./ Шарп Дж., Госни И. Роули А. М.: Мир,1993.204с.
- ДСТУ 4350: 2004 Олії. Методи визначення кислотного числа. Національний стандарт України . Київ. Держспоживстандарт.2007
- ГОСТ 1129 73 Метод определения жирнокислого состава. Межгосударственный стандарт. Минск. Межгосударственный совет по стандартизации, метрологи и сертификации
- ДСТУ ISO 5508- 2001 Жири та олії тваринні і рослинні. Аналізування методом газової хроматографії метилових ефірів жирних кислот (ISO 5508:1990, IDT)
- Брехман И.И. Человек и биологически активные вещества. — М., 1980 ̶ 400 с.
- Метод определения жирнокислотного состава. Межгосударственный стандарт: ГОСТ 30418-96. – [Введ. 01.01.1999]. Минск: Межгосударственньїй совет по стандартизации, метрологии и сертификации, 1996. –9 с.
- ДСТУ 4569: 2006 Жири тваринні і рослинні та олії. . Методи визначення йодного числа. Національний стандарт України. Київ. Держспоживстандарт.2007
- Плахоткін І.В. « Теоретичні основи Технологій харчових виробництв»/ Плахоткін І.В., Тихікова І., Хомич Г. К.:,2006 606с
- Срок годности пищевых продуктов: Расчет и испытание/ Под ред. Р. Стеле; пер.с англ. В. Широкова под. общ. ред. Ю. Г. Базарновой.— СПб.: Профессия, 2006.— 486с., ил., табл., сх..
- Біохімія фенольних сполук / Под. ред..Дж. Харборна М.: Мир,1968̶
- Осип Ю.Л. Хімія ліпідів: методичні вказівки до вивчення курсу-Луцьк: ВНУ ім. Лесі Українки, 20011- 45с.
- ДСТУ ISO 3960-2001 Жири та олії тваринні і рослинні. Визначання пероксидного числа (ISO 3960:1998, IDT)
- Біологічний словник / За ред. К.М. Ситника і В.О. Топачевського. — К., 1986; Боєчко Ф.Ф., Боєчко Л.О. Основні біохімічні поняття, визначення і терміни. — К., 1993; Губський Ю.І. Біологічна хімія. — К.–Тернопіль, 2000.
- Государственная фармакопедия СССР. М.: Медицина. 1968.-258с.
- Набиванець Б.Й. Основи хроматографічного аналізу / Б.И. Набиванець, В.В. Сухан, О.М. Лисенко. – К: Видавничо-полігріфічний центр “Київський університет”, 2002. – 121 с.
- Черньх В.П. Общий практикум по органической химии / В.П. Черных, И.С. Гриценко, М.О. Лозинский, З.И. Коваленко, – Харьков: НФАУ.Золотые страницы, 2002. – 590 с.
- Глубіш П.А. Органічний синтез: навч. посібник. Частинаї. – К: ІЗ МН, 1997. – 320 с.
- Біологічна хімія. Практикум./ Під. Ред. Виноградової Р.П. ̶ К.: Вища школа, 1977 ̶ 384 с
- Шевряков М.В., Яковенко Б.В., Яворенко О.Ф. Практикум з біологічної хімії. ̶ Суми: ВТД « Університетська книга», 2003. ̶ 204 с.
- М.Є.Кучеренко. Ю.Д.Бабенюк. О.М.Васильєв. Р.П.Виноградова. В.М.Войціцький. М.Д.Курський. В.К.Рибальченко. Б.О.Цудзевич. БІОХІМІЯ: Підручник. – К.: Видавничо-поліграфічний центр “Київський університет”, 2002. – 480 с.
ДОДАТОК А
Редакція може не поділяти думку авторів і не несе відповідальність за достовірність інформації. Будь-який передрук матеріалів з сайту може здійснюватись лише при наявності активного гіперпосилання на e-kolosok.org, а також на сам матеріал!