Роботу виконала:
Шевченко Анна Вікторівна,
учениця Cанжариської загальноосвітньої
школи І-ІІ ступенів
Смілянської районної ради
Черкаської області
Керівник:
Коробова Юлія Павлівна,
вчителька біології, хімії
Cанжариської загальноосвітньої
школи І-ІІ ступенів
Смілянської районної ради
Черкаської області,
лауреатка IV Всеукраїнського Інтернет-конкурсу
„УЧИТЕЛЬ РОКУ–2019” за версією
науково-популярного природничого журналу
„КОЛОСОК” у номінації „Хімія”
ВСТУП
Вітамін С належить до важливих життєвонеобхідних аліментарних чинників екзогенного походження, які повинні постійно надходити до організму з продуктами харчування. Дефіцит вітаміну С в організмі, особливо протягом тривалого часу, може зумовити розвиток різних метаболічних розладів. Це стосується, в першу чергу, порушення імунного статусу організму, ферментативних процесів та ряду регуляторних систем, у яких задіяний цей вітамін. Враховуючи важливі біологічні функції вітаміну С, необхідним є достатнє забезпечення ним організму в межах норм фізіологічної потреби. Одночасно з цим, згідно з даними ФАО / ВООЗ, майже у 90% населення більшості країн світу спостерігається дефіцит вітаміну С, глибина якого може сягати 50 і більше відсотків. Це, очевидно, може бути зумовлене як недостатнім вмістом вітаміну С в продуктах харчування, внаслідок руйнування його в процесі зберігання та кулінарної обробки, так і підвищеною потребою, внаслідок психоемоційних і розумових навантажень та дії стресових факторів.
На вміст вітаміну С у харчових продуктах значно впливають тривалість і способи зберігання продуктів, їх кулінарна обробка. Він самий нестійкий з вітамінів, починає руйнуватися вже при нагріванні до 60°С, легко окислюється, особливо при високій температурі, під впливом кисню повітря і в присутності металів (головним чином міді). При різній обробці харчових продуктів тваринного походження вітамін С порівняно швидко руйнується, тому досить важливо знати правильні прийоми їх кулінарної обробки.
Актуальність дослідження обумовлена тим, що вітамін С належить до незамінних аліментарних факторів, які повинні постійно надходити до оргамізму з продуктами харчування. Враховуючи те, що цей вітамін легко руйнується під впливом температури та в присутності кисню, можливий розвиток С – авітамінозних станів при термічній обробці продуктів харчування та недотриманні інших необхідних умов. З огляду на це, вивчення впливу температурного фактора на збереження вітаміну С в продуктах харчування та з’ясування критичних параметрів цього показника, може до певної міри забезпечити надходження вітаміну С до організму в межах рекомендованих норм добової потреби та попередити розвиток вітаміндефіцитних станів.
Мета дослідження. Вивчити вплив високої температури протягом різного періоду часу на вміст вітаміну С в продуктах харчування рослинного походження та оволодіння методом визначення аскорбінової кислоти з використанням індикатора 2,6 – дихлорфеноліндофенола для підтвердження або спростування гіпотези про те, що під впливом високої температури та різнх умов вміст вітаміну С в харчових продуктах рослинного походження змінюється в сторону зменшення.
Завдання:
- дослідити вплив високої температури на вміст вітаміну С в білокачанній капусті протягом різного періоду часу ;
- дослідити вплив високої температури на вміст вітаміну С в картоплі протягом різного періоду часу ;
- дослідити вплив високої температури на вміст вітаміну С в яблуках сорту « Лігольд» протягом різного періоду часу.
Предмет дослідження вивчення впливу високої температури на зміну вмісту вітаміну С в окремих продуктах харчування рослинного походження протягом різного періоду часу.
Об’єкт дослідження: продукти харчування рослинного походження
( білокачанна капуста , картопля, яблука сорту « Лігольд» ) .
Методи дослідження. При опрацюванні методики по визначенню вітаміну С було встановлено, що найбільш придатним для цього є індофенольний метод (метод Тільманса), який дає добре відтворювані результати, (похибка методу <0,05). Одночасно з цим, при визначенні вітаміну С цим методом, слід враховувати деякі особливості. Це стосується як кількості відібраного для визначення біоматеріалу, його попередньої обробки, так і умов проведення експерименту.
Метод є точним і застосовується, як арбітражний. Він використовується для визначення аскорбінової кислоти.
Принцип методу заключається в тому, що аскорбінова кислота відтитровується в кислому середовищі за допомогою реактиву 2,6-дихлорфеноліндофенолу (реактив Тільманса). Цей реактив має в кислому середовищі червоне забарвлення, в нейтральному і лужному середовищі – синє. Друга особливість цього реактиву зводиться до того, що при відновленні він легко переходить в безбарвну лейкоформу.
При титруванні аскорбінової кислоти індофенолом молекула кислоти віддає 2 атоми водню, окислюючись в дегідроаскорбінову кислоту, а молекула індофенолу приєднує 2 атоми водню, відновлюючись в лейкоформу.
Доки йде окиснення аскорбінової кислоти і відновлення фарби, титруюча рідина залишається безбарвною, коли ж окиснення аскорбінової кислоти закінчується і одночасно зупиняється відновлення фарби, перша ж крапля надлишку призводить до появи блідо-червоного забарвлення титрованої рідини, що вказує на закінчення реакції.
Якщо титрування вести за допомогою розчину індофенола певного титру, то по витраті індофенолу можна зробити висновок про кількість аскорбінової кислоти в досліджуваному розчині (1 мл 0,001 н розчину 2,6-дихлорфеноліндофенолу окислює 0,088 мг аскорбінової кислоти) [17:18].
Статистичну обробку матеріалу проводили з використанням програми Microsoft Ехсеl.
Наукова новизна представленої роботи полягає в тому, що в ній зостосовується цілий ряд питань, які раніше не були предметом окремого дослідження. Це, зокрема, зміна вмісту вітаміну С в продуктах харчування тваринного походження під впливом високої температури протягом різного періоду часу.
Практичне значення роботи: отримані результати можна враховувати при консервуванні, приготуванні страв та кулінарній обробці для максимального збереження вмісту вітаміну С в продуктах рослинного походження .
Апробація роботи. Основні результати та матеріали дослідження доповідались і обговорювались на засіданні гуртка «Юний натураліст»
РОЗДІЛ 1. АНАЛІЗ ДАНИХ ЛІТЕРАТУРИ
1.1. Вітамін С та його біологічна роль
1.1.1. Хімічна будова та влвстивості вітаміну С.
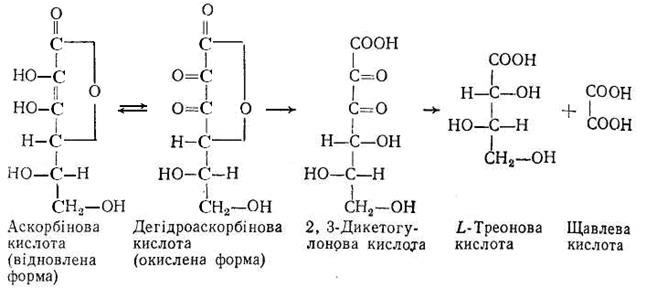
Хімічна природа вітаміну С була остаточно розшифрована у роботах венгерського біохіміка Сент Гіоргі, дослідженнями Хеуорс в Англії і Міхель в Німеччині. Встановлена ними структурна формула вітаміну С, виділеного з природних джерел, підтверджена синтезом, який здійснений у 1933 р. У 1933 р. вітамін С отримав назву аскорбінової кислоти, яка має таку будову:
При дослідженні будови аскорбінової кислоти було встановлено, що вона є похідною L-гулонової кислоти [15:7].
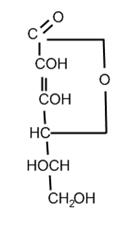
Вітамін С має емпіричну формулу C6 H8 O6, вказуючу на його спорідненість з моносахаридами складу С 6Н 12О6. Будова молекули вітаміну С або аскорбінової кислоти (АК) характеризується відповідно до проекційної формули Толленса:
Вітамін С відповідно до його структури має наступні найменування: γ-лактон 2,3-диенол-L-гулонової кислоти або 4- лактон L-трео-2,3,4,5,6-пентогідрокси-2-гексенової кислоти.
Вітамін С є не кислотою, а лактоном, тобто внутрішнім ефіром 2,3-дегідро-L-гулонової кислоти.
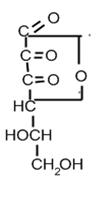
Аскорбінова кислота швидко окислюється до дегідроаскорбінової кислоти (ДАК), що має емпіричну формулу С6Н6О6. У зв’язку з оборотністю цього процесу ДАК володіє антискорбутним ефектом і розглядається часто як друга форма вітаміну С:
З чотирьох можливих ізомерних форм вітаміну С природною, біологічно активною є L-аскорбінова кислота. Решта ізомерів АК одержані синтетично і майже не володіють вітамінними властивостями. Оптична густина L- і D-аскорбінових кислот однакова, але знак обертання поляризованого променя світла, що проходить через розчини, різний. L-аскорбінова кислота обертає площину поляризованого променя світла вправо (/а/D = +23°), D-аскорбінова — на той самий кут вліво. L– і D-ізоаскорбінові кислоти мають дещо меншу оптичну активність, ніж L- і D-аскорбінові кислоти. Відповідно для L-ізомера /а/D = +17° і для D-ізомера /а/D = —17° [16:156].
Антискорбутні властивості аскорбінової кислоти зумовлені наявністю в складі її молекули лактонового циклу. В дослідах з використанням С-аскорбату було виявлено досить виражені редукуючі властивості аскорбінової кислоти. Причому здатність окиснюватись і відновлюватись за рахунок інших сполук пов’язана з наявністю в її складі диенольного угрупування. Окиснення аскорбінової кислоти може здійснюватись, як ферментативно (аскорбатоксидаза), так і не ферментативно (кисень повітря, йони Си2+ і Fе2+).
Першим продуктом окиснення аскорбінової кислоти є дегідроаскорбінова кислота (2,3-дикетогулонолактон). Дегідроаскорбінова кислота залежно від умов може легко відновлюватись в аскорбінову, або ж піддаватись наступному окисненню, внаслідок чого вона перетворюється на дикетогулонову кислоту. Остання далі окиснюється до L-треонової і щавлевої кислоти, які видаляються з організму з сечею. Розщеплення дегідроаскорбінової кислоти проходить спонтанно без участі ферментів [5:71].
ДАК володіє такою ж активністю, як і АК. Очевидно, ця властивість пов’язана із здатністю продукту дегідрування швидко відновлюватися в аскорбінову кислоту. Разом з цим гідратоване похідне ДАК з розкритим кисневим містком — дикетогулонова кислота — не володіє властивостями вітаміну С [3:173].
Дегідроаскорбінова кислота за вітамінними властивостями рівноцінна аскорбіновій, однак вона менш стійка і дуже легко окиснюється з утворенням продуктів, які не мають вітамінних властивостей.
За зовнішнім виглядом аскорбінова кислота біла, кристалічна речовина без запаху, кисла на смак, добре розчинна у воді і не розчинна в жирових розчинниках (бензині, ефірі, хлороформі). 1г кристалічної аскорбінової кислоти розчиняється в 5 мл води, 25мл спирту або 100 мл гліцерину. Температура плавлення аскорбінової кислоти 190°С. В кристалічному стані вона стійка і може зберігатися тривалий час без доступу кисню і вологи.
Водні розчини її, навпаки, малостійкі. Аскорбінова кислота в розчині швидко руйнується, особливо в нейтральному чи лужному середовищі, а також при значному підвищенні температури при наявності йонів важких металів (Си2+, Fе2+). Розчини аскорбінової кислоти приготовлені на бідистильованій воді, що не містить розчиненого кисню та йонів важких металів, не руйнуються навіть при стерилізації в запаяних скляних ампулах. Отримують аскорбінову кислоту в основному синтезом з глюкози та її похідного – спирту сорбіту [5:72].
1.1.2. Ознаки С авітамінозу. Вплив на обмін речовин.
С – авітаміноз (цинга) відома з часів глибокої давнини. Перші описи цинги, як масового захворювання відносяться до XIII ст. Особливо часто страждали мореплавці. Цинга мала широке розповсюдження серед населення різних країн. Тільки за XIX ст. описано 104 епідемії цинги з великою смертністю.
Особливо велике поширення цинга набувала в періоди воєн. Навіть в першу світову війну серед британських військ в Месопотамії хворіли на цингу 30—50% всього складу. Авітаміноз С був масовим захворюванням також і серед цивільного населення, особливо в роки неврожаїв [27:61].
В даний час незрівнянно частіше зустрічаються прояви гіповітамінозу С, головним чином в результаті недбалого відношення до питань контролю за вітамінною повноцінністю харчування. При цьому частіше може виявлятися саме гіповітаміноз С, оскільки даний вітамін легко руйнується, а в організмі людини він не синтезується і не відкладається в запас. Тривале зниження вітаміну С в їжі веде до розвитку явищ гіповітамінозу або навіть авітамінозу. Розвиваються вони найчастіше в зимовий або ранній весняний період, коли вміст вітаміну в харчових продуктах значно знижується. Тривала відсутність вітаміну С протягом 3-5 місяців призводить до розвитку захворювання, що дістало назву цинги, або скорбуту. Явно вираженій формі захворювання передує прихований період з непомітними симптомами, які можуть тривати кілька місяців. Це загальне нездужання, головний біль, постійне відчуття втоми, млявість, порушення сну, апатія, біль у різних ділянках тіла, особливо в м’язах нижніх кінцівок .
Профілактика С- авітамінозу полягає в постійному підтриманні добової потреби організму у вітаміні С. Добова потреба людини у вітаміні С залежить від ряду причин: віку, статі, виконуваної роботи, стану вагітності або годування груддю, кліматичних умов, шкідливих звичок (Додаток А). У зимово-веснняний періоди необхідно проводити індивідуальну профілактику, пов’язану з зниження вмісту вітаміну С в продуктах.
Найхарактернішою ознакою цинги є ураження кровоносних судин, особливо капілярів, яке супроводжується ламкістю їх стінок і підвищенням проникності. Зміни в капілярах призводять до появи підшкірних точкових крововиливів (патехій) [5:72].
При подальшому розвитку захворювання симптоми геморагічного характеру посилюються: густота петехій збільшується не тільки на нижніх кінцівках, але і на шкірі рук, тулуба. Виникають значні крововиливи, посилюються при тривалому лежанні. Мають місце крововиливи в м’язи, особливо в ті, які зазнають механічного навантаження, в суглоби, які опухають, викликають хворобливі відчуття і ускладнюють рухи хворого. Крововиливи з’являються і в кістках: в ребрах вони утворюються в місцях з’єднання їх кістково-хрящової частини і можуть затруднювати подих. Діяльність остеобластів слабшає, остеокласти продовжують руйнувати кістки; кісткова тканина стає тонкою, це може спричинити перелом кістки, що зумовлено значним зменшенням вмісту колагену. Для цинги характерне ураження ясен – гінгівіт, слизова оболонка яких кровоточить, пізніше вона омертвляється, виникають виразки; шийки і корені зубів оголюються, зуби розхитуються; прийом їжі стає важким [38:30].
Усі ці зміни є результатом порушення синтезу основної речовини сполучної тканини, яка за звичайних умов цементує ендотеліальні клітини. Якщо хвороба прогресує, то гемораргічні явища набувають все більшого розвитку. При відсутності в їжі вітаміну С хвороба закінчується смертю. Під час цинги організм людини стає малостійким до різних інфекційних захворювань. Діти, хворі цингою, погано ростуть і розвиваються. Перші симптоми захворювання у них подібні до вищеописаних симптомів для дорослих. Щодо кісткової тканини характерні ураження довгих кісток на межі епіфізів і діафізів, можливе їх відділення один від одного [18:25].
При захворюванні на цингу порушується також діяльність серцево-судинної системи – спостерігаються прискорене серцебиття, болі в ділянці серця, зниження артеріального тиску.
Зміни з боку травного каналу характеризуються катаральним станом слизової оболонки шлунка і кишок, змінюються їх секреторна і моторна функції, розвивається дискенезія ряду внутрішніх органів [5:73].
Біологічна роль аскорбінової кислоти тісно пов’язана з обміном білків, вуглеводів, ліпідів, мінеральних речовин. Так, недостатність вітаміну С в організмі зумовлює порушення обміну амінокислот, зокрема ароматичного ряду. У дітей при нестачі вітаміну С спостерігається підвищення вмісту амінокислоти тирозину в крові. Оскільки вітамін С бере участь в процесах гідроксилювання цілого ряду амінокислот, то при його нестачі має місце порушення синтезу білка колагену, а також еластину. Підвищений вміст білка в раціоні для організмів, що синтезують вітамін С, зумовлює підвищений його синтез та вміст в різних орагнах і тканинах.
Вітамін С впливає на вуглеводний обмін. При нестачі вітаміну С відсутні закономірні зміни концентрації цукру крові, але є інші ознаки , які свідчать про порушення використання в організмі вуглеводів. Досить чітко видно послаблення глікогенної функції печінки і активності деяких ферментів, які каталізують реакції гліколізу: гексокінази, фосфоглюкомутази [5:73]. Це, в свою чергу, зумовлює зниження синтезу глікогену в печінці. Знижена активність гексокінази в шкірі. Ослаблене, також, перетворення вуглеводів в циклі трикарбонових кислот, свідченням цього є виділення з сечею кетонових тіл і лимонної кислоти. Вважають, що вітамін С впливає на вуглеводний обмін через гормони підшлункової залози і наднирників [22:68].
Також, показано, що аскорбінова кислота стимулює окислення глюкози в еритроцитах до СО2 через пентозофосфатний цикл. Виведення глюкози еритроцитами також залежить від забезпеченості організма вітаміном С, при його дефіциті помітно зниження активністі альдози в еритроцитах. При зберіганні законсервованої крові, яка була взята у морських свинок та людей, які отримували з їжею недостатньо вітаміну С, виявлене прискорене зниження здатності еритроцитів виводити глюкозу і швидке зниження їх альдолазної активності [19:387].
Нестача вітаміну С викликає порушення і ліпідного обміну. При С-авітамінозі вміст жирних кислот в тканинах, особливо в печінці, підвищується, а їх синтез із ацетил-КоА знижується. Істотних змін при нестачі вітаміну С зазнає і обмін холестерину. Так, у тварин, які утримувались на атерогенному раціоні і не одержували вітаміну С, відкладання холестерину в різних органах і тканинах було значно вищим, ніж у тварин, що одержували цей вітамін [5:74].
1.2. Поширення вітаміну С в природі
Аскорбінова кислота є одним з найбільш широко поширених в природі вітамінів. Першоджерелом вітаміну С служать головним чином рослини. Людина і тварини отримують його безпосередньо з рослинною їжею і побічно – через продукти тваринного походження, хоча окремі органи мають відносно високі концентрації даного вітаміну. З іншої сторони, насіння і зерна вищих рослин позбавлені вітаміну С. Однак з перших днів проростання в них з’являється аскорбінова кислота. Збагачені вітаміном С листя, плоди, дещо збіднені на нього коренеплоди. Найбільша кількість його міститься в шипшині, грецьких горіхах, чорній смородині, червоному перці, печінці та ін [11:154]. Необхідно звернути увагу на найважливіші джерела вітаміну С нехарчового характеру – шипшину, хвою (сосни, ялини і модрини) і листя чорної смородини. Водні витяжки з них представляють собою майже завжди доступний засіб для попередження і лікування цинги [1:74].
1.2.1. Синтез вітаміну С в організмі людини і тварини.
Потреба в надходженні ззовні готових молекул вітамінів в організм можна розглядати. як окремий випадок гетеротрофіі. Одні види організмів синтезують вітамін C з більш простих речовин і є в цьому відношенні аутотрофними, інші до такого синтезу не здатні і повинні одержувати його з їжею – вони гетеротрофи. Аскорбінову кислоту потребують людина і всі вищі тварини; потрібна вона і рослинам. При цьому рослини і більшість тварин її синтезують. Не здатні до такого синтезу лише людина, вищі антропоїдні мавпи, морські свинки, один вид птахів – червоногузий бульбуля і окремі види летючих мишей. Можна було б думати, що в процесі еволюції здатність до синтезу вітаміну С втрачається. Але виникає питання, чому цю здатність втратили не тільки людина й вищі мавпи, але і морські свинки (представники гризунів), один з видів гороб’ячих птахів та летючі миші, які знаходяться на еволюційних сходах далеко від них? Припускають, що ця втрата – результат мутації, зміни генного апарату, які передаються у спадок і закріплюється у потомстві. Мабуть, під впливом якихось дій у предків людини та інших видів, що потребують екзогенного надходження вітаміну С, випав ген, або кілька генів, які організму забезпечують синтез цих ферментів. Цей генетичний дефект, ця молекулярна хвороба була компенсована включенням в їжу продуктів, у якій є вітамін С, що оберегло ці види від вимирання [20:20].
Чаговець Р.В. розглядає виникнення екзогенності вітамінів не як втрату здатності до їх біосинтезу, а як звільнення від неї. Фонд генів дуже великий, але все таки не безмежний. Чаговець Р.В. підрахував, що для біосинтезу вітамінів необхідно понад 100 різних ферментів. Відсутність необхідності синтезувати ці ферменти вивільняє значну кількість генів. Отже, коли віддалені предки людини втратили здатність в синтезі цих ферментів, у них вивільнявся чималий об’єм генетичного апарату, який міг бути використаний для подальшої еволюції, для вдосконалення виду. Таким чином, потреба в екзогенних вітамінах (так само як і в деяких інших чинниках живлення) з цієї позиції можна розглядати не як негативне явище, а як благо. За тієї умови, що вид зміг пристосуватися до виниклої мутації шляхом зміни характеру живлення: почати споживати їжу, що містить, зокрема, вітамін С [9:205].
В живих організмах аскорбінова кислота утворюється з гексоз за такими двома схемами:
D-глюкози -> D-глюкоронова кислота -> L-аскорбінова кислота
D-галактоза -> D- галактуронова кислота -> L-аскорбінова кислота
L-аскорбінова кислота синтезується з D-глюкози без розірвання його вуглеводного скелету, при цьому перший вуглеводний атом D-глюкози стає шостим в L-аскорбіновій кислоті [32:53].
В людини та окремих тварин не синтезуються деякі ферменти, які перетворють моносахариди в аскорбінову кислоту. У деяких видів птахів і низькоорганізованих ссавців синтез відбувається в печінці та нирках, а у більшості високоорганізованих ссавців – тільки в печінці. У таких тварин цей процес може протікати більш-менш інтенсивно під впливом багатьох факторів. У пацюків біосинтез аскорбінової кислоти гальмується нестачею вітамінів А, В1, В2, Е. Введення хлоретану стимулює синтез. Іншим джерелом аскорбінової кислоти є L-галактонова кислота [15:10].
Було з’ясовано, що гомогенати тканин людини не здатні утворювати аскорбінову кислоту з γ-локтону L-гулонової кислоти, в той час як гомогенати тканин пацюків синтезують вітамін з цього попередника.
Як і всі водорозчинні вітаміни, вітамін C у організмі про запас не відкладається. Незасвоєнний надлишок виводиться з сечею та іншими фізіологічними рідинами. Половина вітаміну С, що надійшов в організм виводиться з нього через 16 діб, тому припинення його введення в організм зумовлює симптоми вітамінної нестачі, які виявляються досить швидко.
Вітамін C засвоюється в кишечнику через канали, керовані іонами натрію. Висока концентрація цукру в кишечнику або в крові погіршує його засвоєння [15:20].
1.2.2. Синтез вітаміну С в рослинах.
Першоджерелом вітаміну С служать головним чином рослини. У них, так само як і в організмі людини і тварин, вітаміни перебувають в активній формі.
Якщо людина і тварини пристосувалися отримувати готові вітаміни з рослин, то рослинам доводиться синтезувати їх з простих сполук. Для цього в ході еволюції вони освоїли складні біохімічні реакції, які проходять з використанням сонячної енергії [30:53].
Процеси, що відбуваються при проростанні насіння, дозволяють їм успішно протистояти несприятливим чинникам зовнішнього середовища, які призводять до утворення в проростках надлишку вільних радикалів. Проте проростаюче насіння успішно нейтралізує їх руйнівну дію за допомогою активного синтезу антиоксидантів. Саме вітамін С є основним антиоксидантом. Кількість саме цього вітаміну збільшується в проростаючому насінні з високою швидкістю [35:101].
Синтез вітамінів і їх накопичення відбувається вже при проростанні насіння. У насінні, в стані спокою, вітамін C не виявлено, а при його проростанні стає справжньою коморою цього “джерела здоров’я”.
Більш всього вітаміну C синтезується в листках рослин, особливо на сонячній стороні. В період підготовки до квітування кількість аскорбінової кислоти досягає максимуму. Під час квітування і плодоутворення в підземних частинах рослин вітаміну C стає все менше і менше, він накопичується в бутонах, квітках, зав’язях і плодах. Стиглі плоди, як правило, найбільш багаті вітаміном C. В період опадання листя цей вітамін в них майже не міститься [10:45].
Синтез аскорбінової кислоти відбувається з використанням сонячної енергії. Тому інтенсивність утворення вітамінів в рослинах підкоряється відомому принципу: чим більше світла і тепла, тим більше “молекул життя”. Вже давно встановлено, що в роки з невеликою кількістю сонячних днів вміст вітаміну C понижений. На швидкість синтезу і збереження аскорбінової кислоти в рослинах позитивно впливає оптимальна забезпеченість їх водою, мінеральними і органічними живильними речовинами. Чим більша вологість грунту, тим швидше відбувається синтез вітаміну С. Фосфорно-калієві добрива підвищують вміст вітаміну С в рослинах, а азотні добрива, навпаки, знижують.
Відомі наступні типи утворення аскорбінової кислоти в рослинах:
1) світловий, тобто залежний від фотосинтезу;
2) незалежнй від світла синтез її в проростаючому насінні;
3) незалежнй від світла, так званий травматичний синтез в поранених органах [21:157].
Багато дослідників вважають, що аскорбінова кислота в організмі рослин синтезується за рахунок цукрів. Проте, питання про конкретну форму цукру, з якого вона синтезується і шляхи його перетворення як і раніше, не з’ясовані. Одні автори вважають, що аскорбінова кислота утворюється в тканинах рослин при участі манози; інші – з глюкози; треті вважають, що синтез вітаміну C в однаковій мірі стимулюється як моно -, так і дицукрами. В даний час вважають, що аскорбінова кислота синтезується в рослинах з D-глюкози і D-галактози незалежними шляхами [21:170].
При утворенні аскорбінової кислоти з D- глюкози використовується L-гулонова кислота, що утворюється з глюкуронової кислоти. Але є ще і запасний шлях синтезу аскорбінової кислоти в рослинах через ступінь утворення, як побічний продукт. 2,3-ендіол-5-оксо-γ-лактона L-гулонової кислоти. Перетворення кетогрупи 5-го вуглецевого атома на вторинноспиртову групу призводить до утворення аскорбінової кислоти [12:1].
1.2.3. Роль та вміст вітаміну C в рослинах за різних умов.
Накопичені за останні десятиріччя факти показують, що вітаміни так само потрібні рослинам як і тваринам. Це не просто побічні продукти їх обміну речовин, а фізіологічно активні речовини, що беруть участь в життєво-важливих процесах. Вияснили, що рослини теж можуть мати вітамінну недостатність, хоча вона й не дуже значна, але якщо додавати вітаміни в грунт або проводити вітамінні підкормки, то це дозволяє помітно підвищувати продуктивність рослин.
Доказом того, що рослинам потрібні вітаміни може бути й такий факт, що при обробці насіння антивітамінами деяких вітамінів, відбувається затримка проростання або ж і зменшення схожості насіння. Також, може відбуватися пригнічення росту органів проростків і, взагалі, загибель проростків [1:60].
Експерименти показують, що за допомогою вітамінів можна керувати деякими процесами: у рослин – посилювати або затримувати їх ріст, прискорювати утворення плодів і т.д.
Добрим і надійним джерелом вітаміну C є дикорослі їстівні трави: борщевик, лобода, кропива, лопух, конюшина, кульбаба, ромашка аптечна, снитка звичайна та інші [1:51].
У рослинах, як і в тваринних організмах, аскорбінова кислота відіграє важливу роль. Віддаючи або приєднуючи атом водню аскорбінова кислота виступає в ролі його переносника, особливо там, де відбувається утворення збагачених енергією молекул АТФ. Тим самим вона служить проміжною ланкою між різними речовинами і реакціями рослинного організму [29:55].
Аскорбінова кислота може бути донором електронів у фотосинтетичних реакціях. Деякими дослідниками було помічено, що більша кількість її накопичується в листках південної крони. Ці факти вказують на те, що під час фотосинтезу синтезується аскорбінова кислота. Отже, вона не тільки впливає на фотосинтетичні процеси, а й сама виникає під час їх проходження. Також вважають, що вона бере участь в перенесенні електронів від пластохінона до цитохрому при фотофосфорилюванні.
Окрім безпосередньої участі аскорбінової кислоти в процесах фотосинтезу, вона може позитивно впливати на асиміляцію вуглекислоти шляхом оберігання хлорофілу від окислення [7:60].
Аскорбіновій кислоті належить важливе значення в диханні рослин. Наявність аскорбінової кислоти у рослин і її участь в дихальній системі додає великої стійкості рослинному організму, оскільки вона може окислюватися різними “кінцевими” оксидазами, тобто може функціонувати в різних умовах температури і на різних етапах розвитку рослин.
Аскорбінова кислота бере участь в мінеральному живленні рослин. Як відомо з деяких літературних даних, при внесенні окремих мінеральних добрив в бідні грунти, у рослинах відмічається збільшення вмісту аскорбінової кислоти. На грунтах з великим вмістом різних елементів мінерального живлення, додавання добрив ефекту не дає. Є такі елементи, при внесенні яких у грунт, вміст аскорбінової кислоти в органах рослин понижується. Таким елементом є азот. Особливо негативно він діє на вміст аскорбінової кислоти в органах плодових дерев. Але внесення бору і мангану збільшує вміст аскорбінової кислоти в листках і коренях петрушки, пастернаку та інших рослин. Цинк і молібден також впливають на збільшення вмісту вітаміну С в різних органах рослин [11:84].
Аскорбінова кислота також бере участь у такому важливому біологічному процесі, як водообмін. Це доказано, наприклад, експериментом, який провели Спірідонова Н. С. і її співробітники над кукурудзою і картоплею у 1968 році. Вони показали, що під дією аскорбінової кислоти посилюється транспірація у рослин, а також швидкість руху води по рослині, так, як аскорбінова кислота сприяє прискоренню цілого ряду метаболічних процесів.
Сорти, що містять велику кількість аскорбінової кислоти, характеризуються підвищеною морозо- і газостійкістю [19:160].
У рослинах, вітамін C знаходиться у складі єдиної окисно-відновної системи, іншим компонентом якої виступає глютатіон. Система аскорбінова кислота – глютатіон найбільш активна в зоні клітинного поділу, тобто вона має безпосереднє відношення до росту рослин.
Беручи участь у всіх окисно-відновних процесах у рослинному організмі, аскорбінова кислота проявляє активуючу дію на ферменти, сприяє нормальному розвитку і підвищенню опірності організму до несприятливих чинників зовнішнього середовища [25:54].
Порівняно багато вітаміну С міститься в зелених частинах деяких дикорослих рослин (Додаток Б). Тут першість належить первоцвіту лікарському – одному з перших весняних квітів, що з’являються на лугах одразу після танення снігу. У листі цієї рослини міститься 700 мг% вітаміну С. Це рекордна кількість, оскільки вміст вітаміну С в листі зазвичай не перевищує 300 мг% [21:159].
1.2.4. Роль та вміст вітаміну С в овочах і фруктах за різних умов.
Щодня ми повинні отримувати 70 мг аскорбінової кислоти з їжею, оскільки вона в організмі про запас не відкладається. Саме овочі та фрукти – єдині і монопольні постачальники вітаміну С. Вони є неперевершиним засобом для нормалізації життєдіяльності корисної кишкової мікрофлори, також нормалізують обмін речовин, особливо жировий і вуглеводний, і попереджають розвиток ожиріння [2:7].
Вміст вітаміну С в їстівній частині різноманітних харчових продуктів, виражений в мг%, тобто в мг на 100 г продукту, представлений в Додатку В.
Вміст вітаміну С в рослинних джерелах може змінюватися при зберіганні. Важливими в харчуванні людини серед овочів є картопля і капуста. Вміст вітаміну С в різних сортах картоплі і капусти різний.
Один і той же сорт в різні роки, за різних метеорологічних умов може також містити різну кількість вітаміну. Вона істотно змінюється від сезону до сезону, наприклад при зборі урожаю, восени, кількість аскорбінової кислоти в картоплі складає 25—30 мг%, до грудня вона знижується до 15—20 мг%, а до березня—квітня падає до 10 мг% і нижче. При зберіганні картоплі протягом 6—8 місяців втрата вітаміну С сягає 50—60%. Проте навіть при незначному вмісті вітаміну С в картоплі остання є важливим його джерелом, оскільки споживається людиною постійно [37:45].
Білокачанна капуста — основне джерело вітаміну С у весняний період. Вона містить досить багато аскорбінової кислоти. Так, наприклад: у лимоні її 40 мг%, а в капусті — 45—60 мг%. І що особливо важливе: до весни в ній зберігається до 30 мг% цього вітаміну, тоді як, наприклад, в яблуках взимку і навесні міститься менше 1 мг% аскорбінової кислоти. Вміст її в капусті неоднаковий в різних сортах. Втрата вітаміну С за 6 місяців зберігання в різних сортах капусти складає 10—40%. У квашеній капусті вітаміну С дещо менше, ніж в свіжій, але все таки навіть навесні вміст його складає не менше 20 мг%. Річ у тому, що при бродінні капусти утворюється вуглекислий газ; він витісняє кисень повітря, що потрапив в діжку при укладанні капусти, і тим самим зберігає вітамін С від руйнування. Зберігати квашену капусту потрібно утрамбованою, покритою розсолом і під вантажем. Інакше кисень руйнуватиме вітамін С. При зберіганні квашеної капусти без розсолу за годину руйнується близько 20% аскорбінової кислоти, за 3 години — більше 30%, а за добу – 70% [2:8].
Інші овочі, що зазвичай споживаються, – морква, буряк, цибуля ріпчата, огірки —по вмісту вітаміну С і по кількості вживання не можуть грати істотної ролі в харчуванні, як джерела вітаміну С.
При зберіганні зелені вміст в ній вітаміну С швидко знижується. Наприклад, за даними Яковлевої Р. Д., вже через 3 години зберігання при температурі 20° шпинат і щавель втрачають 10% вітаміну; через добу зберігання шпинат може втратити до 80% вітаміну С [37:37].
Хрін вживають як гостру смакову приправу в невеликій кількості. Але він не лише підвищує апетит. Завжди хрін цінували і як важливий овоч, в якому містяться до 60 мг% вітаміну С.
Найбільша кількість вітаміну С міститься в плодах шипшини (до 1200 мг%), ягодах чорної смородини (до 200 мг%), червоного перцю (до 250 мг%) [10:48].
Що стосується плодів і ягід, то зазвичай споживані нами сливи. груші, вишні, виноград, журавлина, зібрана восени, — слабкі джерела вітаміну С; те ж саме можна сказати і про більшість сортів яблук. Південні сорти яблук в більшості випадків бідні вітаміном С. Значним вмістом вітаміну відрізняються “Антонівка” і “Тітовка”. За даними Букіна С. Н., в більшості північних сортів яблук, при зберіганні вміст вітаміну С швидко знижується: через 2—4 тижні він вже падає на 60—80%; в пізньостиглих і лежких сортів (наприклад, “Антонівка”) термін таких втрат подовжується до 2—3 місяців. Швидко (за місяць) знижується вміст вітаміну С в таких нележких сортах яблук, як “Білий налив”, “Боровинка” [14:89].
Цитрусові плоди — апельсини, лимони, грейпфрути, мандарини — містять значну кількість аскорбінової кислоти (від 40 мг% у лимонах і мандаринах до 60 мг% у апельсинах і грейпфрутах). Для цитрусових характерним є постійний вміст в цих плодах аскорбінової кислоти, що не змінюється при тривалому їх зберіганні [35:120].
Як джерело вітаміну С звертають на себе увагу плоди шипшини – дикого родича запашної троянди. Вперше вітамін С в шипшині був виявлений ще в 1931 р. німецьким дослідником Ганом, але ще задовго до цього часу плоди шипшини застосовувалися в Росії для лікування кровоточивості ясен, першої ознаки С- авітамінозу [23:265].
Вміст вітаміну С в плодах шипшини різко варіює в різних її видах. Наприклад, є плоди шипшини, які містять на суху вагу лише 100—200 мг% вітаміну С, а є такі, вміст вітаміну С в яких доходить до 15 000 мг% і вище. Зазвичай в рослинних тканинах є фермент аскорбіназа, відкритий Сент-Дьерді. Цей фермент каталізує, подібно до іонів міді і срібла, процес окислення аскорбінової кислоти, тому при зберіганні рослинних і тваринних продуктів вітамін С в них з часом руйнується. У зрілих же плодах шипшини немає аскорбінази, і процес окислення вітаміну йде дуже повільно. Добре і правильно висушені плоди шипшини можуть роками зберегти свою протицинготну активність. Високим вмістом вітаміну С відрізняються наступні види: Rosa cinnamomea (троянда корична) і Rosa acicularis (троянда голчата); Rosa canina (троянда собача), навпаки, відрізняється низьким вмістом вітаміну С [35:125].
Вітамін С добре розчинний у воді; він самий нестійкий з вітамінів, легко окислюється, особливо при високій температурі і у присутності металів (головним чином мідь). Розігрівання і тривале зберігання їжі ведуть до збільшення втрати. Під час смажіння він руйнується в досить не значній кількості. При квашенні продуктів вітамін С зберігається. Після відтаювання свіжозаморожених плодів і овочів вітамін С стає нестійким, тому розморожені продукти потрібно швидко споживати [26:164].
1.3. Вплив фізичних і хімічних факторів на вміст вітаміну С в біоматеріалі
При належному зберіганні вітамін С в своїй вихідній формі зберігає свою біологічну активність протягом ряду років. Добре збереження відзначається також в сухих продуктах. Однак у більш складних умовах (наприклад, при обробці, зберіганні та приготуванні їжі) вітамін піддається впливу ряду фізичних і хімічних факторів, які необхідно приймати до уваги перед вибором збагачуючих компонентів:
– температура, теплова енергія ;
-термін зберігання ;
-вологість ;
-несприятлива величина рН;
-кисень та інші гази ;
-вільні радикали ;
-світло, опромінення ;
– каталізатори (наприклад, іони міді та заліза);
– ферменти [6:57].
Переробка продуктів харчування найбільш сильно впливає на стабільність вітаміну C. Застосування стабілізованих і мікрокапсульованних форм вітамінів значно підвищує їх стійкість у продуктах при різних умовах переробки та зберігання.
Аскорбінова кислота легко руйнується під час технологічної обробки або зберіганні з-за дії металів таких, як мідь чи залізо. Тривалий вплив повітря і нагрівання в присутності кисню руйнує аскорбінову кислоту, таким чином стабільність вітаміну С у збагаченому продукті буде залежати від самого продукту, технології його виробництва, типу використовуваної упаковки. У вітамінізованому продукті або напої зберігається від 75 до 97% вітаміну С при зберіганні 12 місяців при кімнатній температурі [31:100].
Для збільшення стабільності деякі вітаміни можуть піддаватися хімічній модифікації, спеціальній технологічній обробці з метою одержання більш стабільних форм, які дозволяють їх використовувати в різних галузях харчової промисловості. Основні параметри, що враховуються при розробці форм продуктів:
– стабільність (в процесі обробки та при зберіганні) ;
– зручність при використанні (наприклад мінімальне розшарування в кінцевому продукті, стійкість до злежування, хороша сипучість і однорідність);
– розчинність ;
– біодоступність ;
– органолептичні характеристики (наприклад, маскування неприємних запахів за рахунок вмонтування або інкапсулювання діючої речовини в захисну матрицю) [24:144].
Вибір оптимальної упаковки в значній мірі визначається терміном зберігання та вартістю. Вітамін С необхідно захищати від кисню, а рибофлавін і піридоксин – від світла. У напоях, молоці та олії кисень може викликати швидке розкладання вітаміну. Упаковка зі скла – гарний вибір для захисту від кисню, але з точки зору зручності використання, утилізації та інших причин пластмасова є більш прийнятною. Правильно підібрані пакувальні матеріали – шлях до подолання проблем, викликаних взаємодією з киснем. Світлозахисна упаковка (темне скло, темний пластик, асептичні коробки) – також зводять до мінімуму вплив світла і, отже, зведення до мінімуму руйнування світлочутливого вітаміну [36:15].
Більiість фізико-хімічних факторів роблять негативний вплив на стабільність вітамінів, що містяться в продуктах харчування або доданих з метою збільшення поживної цінності. Стабільність цих вітамінів в збагачених продуктах харчування може бути збільшена за рахунок використання відповідної упаковки або певних умов зберігання. Для компенсації втрат в процесі технологічної обробки, зберігання чи поширення, передбачаються певні перезакладки вітамінів, так звані передозування [34:32].
РОЗДІЛ 2. ЕКСПЕРЕМЕНТАЛЬНА ЧАСТИНА
2.1. Матеріали та методи дослідження
Різні овочі і фрукти мають в своєму складі різну кількість аскорбінової кислоти. Для дослідження були відібрані найбільш оптимальні і важливі в харчуванні людини овочі і фрукти з достатнім вмістом вітаміну. Для вивчення впливу високої температури на вміст вітаміну С були використані: овочі- бульби картоплі, білокачанна капуста; фрукти – яблука сорту “Лігольд”. Хоч картопля в своєму складі містить не досить багато вітаміну С, але якщо врахувати, що цей продукт вживається майже щоденно в достатній кількості, то людина в значній мірі забезпечується вітаміном С за рахунок картоплі, якщо він не руйнується і не втрачається при дії високих температур (варінні).
Існують різні методи визначення вітаміну C в біологічному матеріалі: полярографічний, колориметричний, флуориметричний, метод візуального титруванням (оксидометричний). Останній, запропонований І. Тільмансом, має кілька модифікацій і внаслідок своєї доступності отримав найбільше поширення (метод Тільманса).
В досліджуваному біоматеріалі концентрацію вітаміну С ми визначали саме методом Тільманса, який дає відтворювані результати (похибка методу <0,05).
Принцип методу визначення вітаміну С грунтується на редукуючій здатності цього вітаміну. При його визначенні використовують окисно-відновну реакцію між аскорбіновою кислотою і 2,6 – дихлорфеноліндофенолом в кислому середовищі. Цей реактив використовується в даному методі не тільки як окислювач, але і як індикатор, за яким можна встановити завершення титруванням. При цьому інтесивно пофарбований реагент переходить в безбарвну лейкоформу [17:18].
2,6-дихлорфеноліндофенол (індикатор) показує два види реакції. Один вид обумовлюється зміною pH середовища, як у звичайних ацидометричних індикаторів; при цьому відбувається перехід від інтенсивного синього кольору в лужному середовищі до блідо-червоного – в кислому середовищі. Перехід забарвлення відбувається між рН 4 і 5, в цьому інтервалі індикатор має фіолетовий колір. Другий вид реакції – це ОВ-перехід від темно-синього окисленого стану до безбарвного. Цю останню реакцію і використовують для визначення аскорбінової кислоти.
Кількісне визначення вітаміну С проводили, шляхом титрування досліджуваного розчину підкисленоuj соляною кислотою, лужним розчином 2,6-дихлорфеноліндофенола. Поки в титруючому розчині міститься вітамін С, лужний розчин 2,6-дихлорфеноліндофенола, що додається, буде знебарвлюватися за рахунок утворення відновленої форми аскорбінової кислоти. Як тільки вся кількість вітаміну С, наявна в досліджуваному розчині, окислеться, 2,6-дихлорфеноліндофенол не буде відновлюватися і титруючий розчин набуває рожеве забарвлення за рахунок переходу лужного розчину 2,6-дихлорфеноліндофенола синього кольору в 2,6-дихлорфеноліндофенол червоного кольору в кислому середовищі.
Кислотні витяжки з рослин титрували розчином індикатора (відомого титру) до настання рожевого забарвлення, обумовленого надлишком індикатора в кислому середовищі. На одну молекулу аскорбінової кислоти (молекулярну масу 176) припадає дві молекули індикатора.
Точність методу багато в чому залежить від застосовуваної техніки аналізу. Так як аскорбінова кислота є дуже лабільною речовиною, то в розтертій рослинній тканині вона швидко окислюється, перетворюючись на дегідроаскорбінову кислоту. Тому всі операції, пов’язані з взяттям середньої проби матеріалу для аналізу, подрібнення і розтирання наважки і т.п., повинні бути виконані досить швидко.
Дослідження впливу високої температури на вміст аскорбінової кислоти в біоматеріалі проводилися в різних умовах: при відкритому та закритому посуді та протягом різного часу. Такий принцип роботи застосовували для отримання більш повних результатів та вияснення, pf яких саме умов в овочах та фруктах зберігається більше вітаміну С.
Обладнання та реактиви .
Обладнання: мікробюретка, мірний циліндр, хімічні стакани на 20 мл, лійка, скляна паличка, ступка, ніж, електрична плитка, колбочки на 50-100 мл, вата для фільтрування, піпетки на 5 мл, аналітичні терези.
Реактиви: 0.001 н розчин 2,6-дихлорфеноліндофенол (реактив Тільманса), 2% розчин хлоридної кислоти, дистильована вода.
2.2. Схема дослідження
Спочатку проводилася серія дослідів при відкритому посуді.
- Біоматеріал, а саме: бульби картоплі та яблука, очищали для взяття середньої проби.
- Досліджуваний матеріал поміщали в термостійкий посуд, заливали водою і ставляли на електричну плитку.
- Впливу високої температури на вміст вітаміну C вивчали протягом 10 хв; 20 хв; 30 хв; 60 хв кипіння.
- Після кожного разу 5 г наважки біоматеріалу розтирали у фарфоровій ступці до отримання однорідної маси. До неї поступово додавали 15 мл 2% розчин хлоридної кислоти. Одержану витяжку фільтрували в мірну колбу через вату. До 3 мл фільтрату додавали 2-5 мл дистильованої води і титрували з мікробюретки 2,6-дихлорфеноліндофенолом до появи стійкого слабко-рожевого забарвлення, яке не зникало протягом 10-15 сек. Титрування повторювали, як мінімун 3 рази для отримання більш точного результату.
1 мл 0,001 н розчину 2,6-дихлорфеноліндофенолу відповідає 0,088 мг аскорбінової кислоти.
Потім проводили серію дослідів при закритому посуді, дотримуючись всіх вимог попередніх умов.
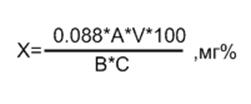
Вміст аскорбінової кислоти в досліджуваному біоматеріалі розраховували за формулою:
Х – вміст аскорбінової кислоти ;
0,088 – кількість мг аскорбінової кислоти, що відповідає 1 мл точного 0,001 н. розчину реактиву Тільманса;
А- кількість 0,001 н розчину 2,6-дихлорфеноліндофенолу, затраченого на титрування, мл;
V- загальний об’єм фільтрату, мл;
В- кількість фільтрату, взятого для титрування, мл;
С- наважка, г.
РОЗДІЛ 3. РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ ТА ЇХ ОБГОВОРЕННЯ
3.1. Вплив високої температури на динаміку вмісту вітаміну С в овочах
Дослідження впливу високої температури на зміну вмісту вітаміну С в овочах та фруктах проводилися в зимово-весняний період. Саме в цей період найчастіше спостерігаються підвищенння проявів гіповітамінозу С. Однією з причин якого є – зниження вмісту вітаміну С в продуктах рослинного походження.
Крім того на вміст вітаміну С у харчових продуктах значно впливає тривалість та способи їх зберігання, а також їх кулінарна обробка, а саме тривалість впливу високої температури.
Враховуючи важливе значення вітаміну С, як незамінного аліментарного чинника, а також те, що він є нестійким і легко руйнується під впливом температури, в першій серії дослідів ми поставили за мету вивчити вплив високої температури на вміст аскорбінової кислоти в бульбах картоплі протягом різного періоду часу при відкритому посуді (табл. 3.1.).
Як видно з даних таблиці, вміст вітаміну С в бульбах картоплі до нагрівання (контроль) складає 4,16 мг%. При нагріванні до 100оС спостерігається уже незначне зниження вітаміну С – 3,56 мг%. При кип’ятінні протягом 10 хв – ці зміни були суттєвішими. Вміст вітаміну в порівнянні з контролем знизився на 34,4%. Подальше кип’ятіння зумовлювало більш значне руйнування вітаміну С в бульбах картоплі. Так, при кип’ятінні протягом 30 хв вміст вітаміну С знизився на 45,2%, а протягом 60 хв – на 50%.
За деякими літературними даними, швидкість руйнування вітаміну С при температурі 50-55 оС в 2-3 рази вища, ніж при 25-30 оС.
В другій серії дослідів ми ми поставили за мету вивчити вплив високої температури на вміст аскорбінової кислоти протягом різного періоду часу в закритому посуді (табл. 3.2.). Ці результати свідчать, що за цих умов тривале нагрівання бульб картоплі зумовлює менш істотне зменшення вітаміну С. Так, при нагріванні до 100оС вміст вітіміну С складав 3,78 мг%, що на 9,1% менше порівняно з контролем, це свідчить про те, що вже на початкових етапах впливу високої температури втрати вітаміну С значно нижчі від показників отриманих при відкритому посуді. При кип’ятінні протягом 10 хв вміст даного вітаміну С порівняно з контролем знизився на 18,3 %, при кип’ятінні протягом 30 хв – на 34,9%, а при кип’ятінні протягом 60 хв – на 46,6%.
Тобто, як видно з навединих даних, втрати вітаміну С є суттєвішими при кип’ятінні у відкритому посуді. Це очевидно зумовлено тим, що вітамін С легко окиснюється і переходить в дегідроаскорбінову кислоту, яка далі руйнується з утворенням сполук для яких не характерні вітамінні властивості (2,3 – дикетогулонова кислота, треонова та щавлева).
Таблиця 3.1.
Вплив високої температури на вміст аскорбінової кислоти в бульбах картоплі при відкритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
4,16+ 0,008
100
|
3,56+ 0,015
< 0,05
85,3
|
2,73+ 0,012
< 0,05
65,6
|
2,42+ 0,015
< 0,05
58,2
|
2,28+ 0,011
< 0,05
54,8
|
2,08+ 0,021
< 0,05
50
|
Таблиця 3.2.
Вплив високої температури на вміст аскорбінової кислоти в бульбах картоплі при закритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
4,16+ 0,008
100 |
3,78+ 0,010
< 0,05
90,9
|
3,40+ 0,009
< 0,05
81,7 |
3,12+ 0,041
< 0,05
75 |
2,71+ 0,008
< 0,05
65,1 |
2,22+ 0,012
< 0,05
53,4 |
При порівнянні показників вмісту вітаміну С, що були отримані під впливом високої температури за різних умов, встановлено високі значення достовірності між середніми показниками вмісту вітаміну С. Висока вірогідність різниці спостерігалася між всіма середніми значеннями вибірок порівняно з контролем.
В третій серії дослідів ми поставили за мету вивчити вплив високої температури на вміст аскорбінової кислоти в білокачанній капусті протягом різного періоду часу при відкритому посуді (табл. 3.3.).
Як видно з даних таблиці, вміст вітаміну С в білокачанній капусті до нагрівання (контроль) складав 4,31 мг%. При нагріванні до 100оС вміст вітаміну знизився на 4,9%, порівняно з контролем, і складав 4,10 мг%. При кип’ятінні 10 хв втрати вмісту вітаміну С були суттєвішими і складали 3,56 мг%. Подальше кип’ятіння зумовлює не значне зниження показників. Так, при нагрівання протягом 30 хв вміст вітаміну С знизився на 23,4%, а при нагріванні протягом 60 хв – на 26,7%.
В таблиці 3.4. наведені дані, отримані при дослідженні впливу високої температури на вміст вітаміну С в білокачанній капусті протягом різного періоду часу при закритому посуді. За цих умов спостерігається значна відмінність цих показників від отриманих в попередньому дослідженні, що зумовлено відсутністю вільного доступу кисню повітря. Так, при нагріванні до 100оС вміст вітаміну С складав 4,25 мг%. При кип’ятінні протягом 10 хв вміст вітаміну знизився на 12,3% порівняно з контролем, при кип’ятінні протягом 30 хв – на 17,5%. Кип’ятіння протягом 60 хв на 21,6% зменшує вміст вітаміну С порівняно з контролем.
При порівнянні показників вмісту вітаміну С, що були отримані під впливом високої температури за різних умов, встановлено високі значення достовірності між середніми показниками вмісту вітаміну С. Висока вірогідність різниці спостерігалася між всіма середніми значеннями вибірок порівняно з контролем.
Таким чином, одержані дані свідчать про те, що для збереження вітаміну С в бульбах картоплі та білокачанній капусті, при їх кулінарній обробці доцільно дотримуватися певних умов, зокрема готувати продукти при закритому посуді.
Таблиця 3.3.
Вплив високої температури на вміст аскорбінової кислоти в білокачанній капусті при відкритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
4,31+ 0,011
100 |
4,10 + 0,005
< 0,05
95,1 |
3,56+ 0,013
< 0,05
82,6 |
3,40+ 0,009
< 0,05
78,9 |
3,30+ 0,010
< 0,05
76,6 |
3,16+ 0,006
< 0,05
73,3 |
Таблиця 3.4.
Вплив високої температури на вміст аскорбінової кислоти в білокачанній капусті при закритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
4,31+ 0,011
100 |
4,25+ 0,006
< 0,05
98,6 |
3,78+ 0,019
< 0,05
87,7 |
3,65+ 0,009
< 0,05
84,7 |
3,56+ 0,013
< 0,05
82,5 |
3,38+ 0,011
< 0,05
78,4 |
3.2. Вплив високої температури на руйнування вітаміну С в фруктах
В першій серії дослідів ми поставили за мету вивчити вплив високої температури на вміст вітаміну С протягом різного періоду часу в яблуках сорту “Лігольд” при відкритому посуді (табл. 3.5.).
Як видно з даних таблиці, вміст аскорбінової кислоти в яблуках до нагрівання (контроль) складає 2,35 мг%. При нагріванні до 100оС вміст вітаміну знизився на 6%, порівняно з контролем, і складав 2,21мг%. При кип’ятінні протягом 10 хв вміст вітаміну знизився до 2,01 мг%. Подальше кип’ятіння зумовлювало суттєвіше руйнування вітаміну С. Так, при кип’ятінні протягом 20 хв вміст вітаміну С знизився на 27,7%, а протягом 60 хв – на 63,9% і складав 0,85 мг%.
В другій серії дослідів ми поставили за мету вивчити вплив високої температури на вміст вітаміну С в яблуках сорту “Лігольд” протягом різного періоду часу при закритому посуді (табл. 3.6.).
Отримані результати свідчать про те, що за цих умов тривале кип’ятіння яблук зумовлює менш істотне зменшення вітаміну С. Так, при нагріванні до 100оС вміст вітаміну складає 2,29 мг%, при кип’ятінні протягом 20 хв – 1,86 мг%, що на 20,9% менше порівняно з контролем. Кип’ятіння протягом 60 хв призводить до зменшення вітаміну С на 41,7% і складає 1,37 мг%.
При порівнянні показників вмісту вітаміну С, що були отримані під впливом високої температури за різних умов, встановлено високі значення достовірності між середніми показниками вмісту вітаміну С. Висока вірогідність різниці спостерігалася між всіма середніми значеннями вибірок порівняно з контролем.
Таким чином, як видно з навединих даних втрати вітаміну С є суттєвішими при кип’ятінні у відкритому посуді.
Таблиця 3.5.
Вплив високої температури на вміст аскорбінової кислоти в яблуках сорту “Лігольд” при відкритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
2,35+ 0,008
100 |
2,21+ 0,005
< 0,05
94 |
2,01+ 0,020
< 0,05
85,5 |
1,70+ 0,010
< 0,05
72,3 |
1,62+ 0,012
< 0,05
68,9 |
0,85+ 0,02
< 0,05
36,1 |
Таблиця 3.6.
Вплив високої температури на вміст аскорбінової кислоти в яблуках сорту “Лігольд” при закритому посуді, мг%
|
Статистичний показник |
Контроль |
Дослід |
||||
|
Нагрівання до 100оС |
Тривалість кипіння |
|||||
|
10 хв. |
20 хв. |
30 хв. |
60 хв. |
|||
|
М ± m
р
% |
2,35+ 0,008
100 |
2,29+ 0,005
< 0,05
97,4 |
2,13+ 0,008
< 0,05
90,6 |
1,86+ 0,015
< 0,05
79,1 |
1,69+ 0,015
< 0,05
71,9 |
1,37+ 0,015
< 0,05
58,3 |
РОЗДІЛ 4. ДОТРИМАННЯ ПОЛОЖЕНЬ З ПИТАНЬ ОХОРОНИ ПРАЦІ ПРИ ВИКОНАННІ НАУКОВО – ДОСЛІДНОЇ РОБОТИ В БІОХІМІЧНІЙ ЛАБОРАТОРІЇ ННІ ПРИРОДНИЧИХ НАУК
4.1.Загальні положення
- В біохімічній лабораторії повинні бути наявні інструкції з техніки безпеки, затверджені адміністрацією.
- До роботи в біохімічній лабораторії можуть бути допущені особи після детального вивчення правил техніки безпеки та проведеного інструктажу відповідальною особою.
- В лабораторії повинні бути наявні засоби особистого захисту (халати, гумові рукавички, захисні окуляри), засоби для надання першої медичної допомоги (медична аптечка, укомплектована необхідними препаратами), протипожежні засоби (вогнегасник, пісок, вода).
- В лабораторії заборонено вживати їжу, палити. Працювати слід у спецодязі (халатах).
- Роботи, пов’язані з виділенням газів та випарів, проводити лише під витяжною шафою.
- Відбирати розчини потрібно лише піпетками, використовуючи спеціальні пристосування з гумовими грушами або дозатори, а не набирати розчини через піпетку ротом.
- Для приготування розчинів сипкі речовини відбирають шпателем, кількісно переносять в мірні стакани чи колби. Готові реактиви зберігають у закритому посуді з етикетками, на яких вказують формулу сполуки, концентрацію та дату приготування.
4.2. Реактиви та поводження з ними
- При роботі з реактивами слід враховувати їх властивості. Оскільки вони можуть бути токсичні, отруйні, шкідливі. Хімічні реактиви не можна брати руками та пробувати на смак!
- Зберігати реактиви слід у спеціально обладнаних приміщеннях, де наявна витяжна система. Окремо слід зберігати кислоти і луги, леткі речовини, органічні і неорганічні. Щоб запобігти руйнуванню паперових етикеток при тривалому зберіганні реактивів, їх необхідно покривати парафіном.
- Деякі реактиви здатні до самозаймання (білий і жовтий фосфор, пірофорні метали, металоорганічні сполуки, зокрема етил-алюміній). До вогненебезпечних відносять також ефіри (диетиловий, аміловий), спирти (етиловий, бутиловий, метиловий), вуглеводні (бензин, петролейний ефір), ароматичні сполуки (бензол, толуол, ксилол), сірковуглець, ацетон. Не слід зберігати поруч реактиви здатні при взаємодії самозайматися або виділяти велику кількість тепла (металічний натрій, калій, літій). Білий фосфор не можна зберігати поруч з вогненебезпечними речовинами). Бертолетову сіль, KMnО4, Na2О2, Н2О2, НСІО4 та інші окисники не слід зберігати разом з відновниками – сіркою, вугіллям, крохмалем, фосфором. Речовини, здатні до самозаймання, слід зберігати у спеціальній тарі. Не слід змішувати і розтирати бертолетову сіль, KMnО4, Н2О2 та інші окисники з органічними реактивами. Обережно слід поводитись з хлорною кислотою та її солями, так як випари цієї кислоти можуть вибухати при контакті з органічними речовинами та речовинами, які легко окиснюються (солями трьохвалентної сурми), а солі хлорної кислоти можуть вибухати без видимих причин.
4.3. Вимоги безпеки в аварійних ситуаціях
При виникненні аварійної ситуації необхідно:
- Повідомити наукового керівника та персонал лабораторії.
- Відключити від джерела живлення всі прилади та обладнання.
- Залежно від характеру аварійної ситуації застосувати необхідні засоби захисту.
4.4. Перша медична допомога в лабораторії
- При незначних забиттях до постраждалого органу прикласти холодний компрес, при порізах відкритих ділянок шкіри не торкатися рани руками та сторонніми предметами, накласти стерильну пов’язку та забинтувати.
- При порізах та пораненнях склом необхідно видалити залишки скла з порізу та обробити рану йодом і перев’язати поранене місце бинтом. При роботі в лабораторії внаслідок необережності можуть статися хімічні і термічні опіки, отруєння випарами різних хімічних реактивів. Виникає необхідність надання першої медичної допомоги постраждалим. Для цього у кожній лабораторії повинні бути аптечка або такі набори: 1) бинт, 2) гігроскопічна вата, 3) 3%-ний розчин йоду, 4) 2%-ний розчин Н3ВО3, 5) 2%-ний розчин СН3СООН, 6) 3%-ний розчин NаНСО3 (питна сода), 7) колодій або клей БФ.
- При термічних опіках першого та другого ступеня слід зробити примочки із 2%-ного свіжоприготовленого розчину NаНСО3 або 5%-ного розчину КМnО4. Ефективним є застосування 96%-ного етилового спирту, який виявляє знезаражуючу дію. При більш тяжких опіках слід звернутися до лікаря.
- При хімічних опіках (кислотами, лугами) вражену ділянку швидко промивають великою кількістю води, а потім, при опіках кислотою, роблять примочки із 2%-ного розчину NаНСО3, а при опіках лугами – 2%-ного розчину СН3СООН. При потраплянні на шкіру кислот чи лугів, вражені ділянки промити відповідно 1%-ним розчином NаНСО3 або 1%-ним водним розчином СН3СООН, а потім змити струменем води. При потраплянні кислоти або лугу на слизові оболонки та органи зору їх слід промити великою кількістю води та звернутися за медичною допомогою. При отруєнні хімічними реактивами слід надати першу допомогу із використанням запобіжних засобів та звернутися до лікаря.
- При ураженні електричним струмом слід негайно відключити струм, відокремити постраждалого від струмопровідних частин, ізолювавши руки гумовими рукавичками. Потерпілому надати зручної пози, розстібнути одяг, створити приплив свіжого повітря, забезпечити цілковитий спокій, слідкувати за пульсом та диханням. У важких випадках зробити штучне дихання та негайно викликати швидку допомогу.
4.5. Дотримання правил техніки безпеки при проведенні експерименту
При проведенні експериментального наукового дослідження по виконанню наукової роботи ми дотримувалися правил техніки безпеки, рекомендованих для роботи в біохімічній лабораторії.
Перед початком роботи науковим керівником було проведено інструктаж з питань охорони праці та співбесіду з керівником по дотриманню правил техніки безпеки при роботі з хімічними реактивами, біоматеріалом, приладами обладнанням. Було перевірено наявність та стан засобів індивідуального захисту.
При виконанні роботи користувалися приладами та обладнанням сертифікованими для використання в Україні, при наявності документів, які засвідчують їх технічний стан. Перед використанням приладів детально вивчали інструкцію, перевіряли наявність заземлення та відсутність ушкоджень.
При роботі з біоматеріалом (кров, сеча) слід користувалися засобами індивідуального захисту (гумовими рукавичками), не допускаючи потрапляння біоматеріалу на шкіру та слизові оболонки. Відбирали біоматеріал за допомогою гумових груш, автоматичних піпеток, дозаторів. Всі матеріали та обладнання, які використовуються при роботі з біоматеріалом були одноразового використання.
У випадку потрапляння біоматеріалу на шкіру, її обробляли тампоном, змоченим розчином пероксиду водню, або іншими дезинфікуючими засобами (1% розчином борної кислоти). Якщо кров потрапила на слизові оболонки, їх промивали великою кількістю води та дезинфікуючими засобами.
Перед проведенням наукового дослідження ретельно вивчали методику та готували робоче місце і реактиви.
4.6. Вимоги безпеки після завершення роботи в лабораторії
Після завершення роботи вимикали від мережі живлення прилади та обладнання, воду та електроенергію.
Приводили в порядок робоче місце та в належний стан засоби індивідуального захисту.
Слідкували за дотриманням гігієнічних умов, систематично мили руки теплою водою з милом.
ВИСНОВКИ
- При дослідженні впливу високої температури на вміст вітаміну С в овочах та фруктах, було встановлено, що висока температура негативно впливає на збереження цього вітаміну, про що свідчать значні втрати його.
- Втрати вітаміну С залежать від тривалості дії температурного фактора, а також умов нагрівання. Суттєвішими є втрати вітаміну при кип’ятінні протягом 30, 60 хв у присутності кисню.
- При порівнянні збереження вітаміну С при високих температурах встановлено, що в овочах, а саме в бульбах картоплі, втрати значніші, ніж у фруктах.
- Виявлено негативний вплив температури на збереження вітаміну С навіть при не тривалому нагріванні, що очевидно зумовлене гідролітичним руйнуванням циклічної структури.
- Отримані результати дають підстави припустити, що явище С- авітамінозу у значній мірі може залежати не лише від недостатнього надходження вітаміну С в організм, але і при руйнуванні його внаслідок тривалого зберігання та кулінарної обробки.
СПИСОК ВИКОРИСТАНИХ ДЖЕРЕЛ
- Акопов И.Э. Важнейшие Отечественные лекарственные растения и их применение / И.Э.Акопов. – М.: Высшая школа, 1990. – 150 с.
- Антосик А. В. Вітаміни – важлива складова овочів та фруктів / А.В. Антосик // Дім, сад, город. – 2002. – №1. – С.7-10.
- Березов Т.Т. Биологическая химия / Т.Т. Березов, Б.Ф. Коровкин. М.: Медицина, 1983. – 253 с.
- Богданов Н.Г. Витамин С / Н.Г. Богданов // Здоровье. – 1982. – №12. – С.9-12.
- Боєчко Л.О. Вітамін С (аскорбінова кислота) / Л.О. Боєчко // Основи біохімії вітамінів та гормонів. – Черкаси: Видаництво ЧНУ, 2005. – С.70-75.
- Ведрашко В.С. Витамины круглый год / В.С. Ведрашко. – М.: Россельхозиздат, 1985. – 96 с.
- Гаммерман А.Ф. Лекарственные растения – источники витамина С. / А.Ф. Гаммерман // Лекарственные растения. – М.: Высшая школа, 1990. – С. 58-80.
- Гельгор В.М. Аскорбиновач кислота / В.М. Гельгор // Химия и жизнь. – 1978. – №3. – С.38-41.
- Горбачев В. В. Витамины, микро- и макроэлементы. Справочник / В.В. Горбачев, В.Н. Горбачева. – Мн.: Книжный Дом; Интерпрессервис, 2002. – 544 с.
- Гром И.И. Источники витамина С / И.И. Гром // Растения – витаминоносители. – М.: Медицина, 1970. – С.45-53.
- Гринкевич Н.И. Лекарственные растения / Н.И. Гринкевич. – М.: Высшая школа, 1991. – 234 с.
- Грузинов Е.В. Поговорим о витаминах / Е.В. Грузинов // Химия. – 1998. – № 24. – С.1-3.
- Девятнин В.А. Методы определения витаминов (химические и биологические) / В.А. Девятин, В.М. Иосиков. – М.: Колос, 1954. – 260 с.
- Ефремов В.В. Аскорбиновая кислота (витамин С) / В.В. Ефремов, К.С. Петровский // Гигиена питания. – М.: Медицина, 1971. – Т.1. – С.89-98.
- Зенгбуш П.К. Витамины и их роль в метаболизме высших и низших организмов / П.К. Зенгбуш // Молекулярная и клеточная биология. – М.: Наука, 1982. – Т.І. – С.5-23.
- Колотилова А.И. Витамин С / А.И. Колотилова, Е. П. Глушанков // Витамины (химия, биохимия и физиологическая роль). – Л.: Изд-во Ленингр. Ун-та, 1976. – С.155-178.
- Кулис Ю.Ю. Определение аскорбиновой кислоты анализатором в биологических средах / Ю.Ю. Кулис, А.А. Друнгилене // Журнал аналитической химии. – 1990. – Т.45. №10. – С.18-20.
- Кушко В.М. Витамин С. / В.М. Кушко // Витамины и здоровье. – М.: Медицина, 1966. – С.24-29.
- Матусис И.И. Витамин С (аскорбиновая кислота) / И.И. Матусис, М.И. Смирнов // Витамины. – М.: Медицина, 1974. – С.384-414.
- Мочалова И.А. Биологическая роль витаминов и их источники / И.А. Мочалова // Химия в школе. – 1998. – №6. – С.19-24.
- Муравьёва Д.А. Витамин С в растених / Д.А. Муравьёва, И.А. Самылина , Т.П. Яковлев // Фармакогнозия. – М.: Медицина, 2002. – С.157-172.
- Неверов И.В. Место антиоксидантов в комплексной терапии пожилых больных / И.В. Неверов // Русский медицинский журнал. – 2001. – Т. 9, № 18. С.67-75.
- Пашутин Д.Н. Витамин С (аскорбиновая кислота) / Д.Н. Пашутин // Химия витаминов. – М.: Пищепромиздат, 1972. – С. 265-278.
- Подколозин А.А. Витамин С / А.А. Подколозин, К.Г. Гуревич // Действие биологически активных веществ в малых дозах. – М.: КМК, 2002. – С.144-153.
- Покровский А.А. Метаболические аспекты фармакологии и токсикологии пищи / А.А. Покровский. – М.: Медицина, 1979. – 184 с.
- Полинг Л. Витамины / Л. Полинг. – М.: Медицина, 1965. – С. 245.
- Романовский В.Е. Витамин С (аскорбиновая кислота) / В.Е. Романовский, Е.А. Синькова // Витамины и витаминотерапия. – Ростов-на-Дону: Феникс, 2000. – С.59-73.
- Романовский В.Е. Витамины и витаминотерапия / В.Е. Романовский, Е.А. Синькова // Медицина для вас. – Ростов-на-Дону: Феникс, 2000. – С. 320-335.
- Северин Е.С. Витамин С / Е.С. Северин // Биохимия. – М.: Геотар – Мед, 2003. – С.254-267.
- Синяков А.Ф. Витаминные растения / А.Ф. Синяков // Рецептя для здоровья. – М.: Наука, 1986. – С.53-57.
- Скурихин И.М. Всё о пище с точки зрения химика / И.М. Скурихин, А.П. Нечаев. – М.: Высшая школа, 1991. – 288 с.
- Спиричев В.Б. Где взять витамины? / В.Б. Спиричев // Химия и жизнь. – 1988. – №9. – С.50-54.
- Спиричев В.Б. Ещё раз о витамине С / В.Б. Спиричев // Здоровье. – 1989. – №5. – С.22.
- Спиричев В.Б. Теоритичиские и практичиские аспекты современной витаминологии / В.Б. Спиричев // Украинский биохимический журнал. – 2004. – Т. 76, № 4. – С. 32 – 49.
- Тюренкова И.Н. Растительные источники витаминов / И.Н. Тюренкова. – Волгоград: Высшая школа, 1999 год. – 158 с.
- Хольст А.О. О содержании витамина С в готовых блюдах / А.О. Хольст, Л. М. Фрелих // Здоровое питание. – 1958. – №2. – С. 15-20.
- Шарманов Т. Белковое питание и витамин С / Т. Шарманов, А. Алдашев. – Алма-Ата: Казахстан, 1934. – 108 с.
- Ярусова Н.С. О витамине С (аскорбиновой кислоте) и С – витаминизации пищи / Н.С. Ярусова. – М.: Медгиз, 1960. – 58 с.
Додатки
ДОДАТОК А
Таблиця А1.
Рекомендована добова потреба організму в вітаміні С [28:322]
|
Категорії |
Вітамін С, мг |
|
Діти: до 1 року до 3 років до б років до 10 років до 17 років Чоловіки (залежно від фізичної активності) Жінки: вагітні в період лактації Люди похолого віку |
30-40 45 80 60 70 70 -100
70 – 80 90-100 110-120 80 |
ДОДАТОК Б
Таблиця Б1.
Вміст вітміну С в зелених частинах дикорослих рослин в мг% [21:159]
|
Дикорослі рослини |
Вітамін С |
|
Первоцвіт лікарський Фіалка трибарвна Листя брусниці Хвоя сосни, ялини Люцерна Листя суниці Верблюжа колючка Лобода біла Кропива дводомна Борщевик дрібнолистий Снитка їстівна Борщовик крупнолистий |
700 290 до 270 250 225 120-200 180 150 100 75 70 25-50 |
ДОДАТОК В
Таблиця В1.
Вміст вітаміну С в різних його джерелах [28:324]
|
Овочі |
Вміст аскорбінової к-ти, мг% |
Фрукти |
Вміст аскорбінової к-ти, мг% |
|
Баклажани Бруква Зелений горошок Кабачки Капуста червонокачанна Капуста кольорова » кольрабі Капуста білокочанна Картопля Цибуля зелена » ріпчастий » порей Морква червона Огірки Перець червоний, солодкий і гіркий Петрушка, листя Редис Редька Ріпа Салат темно-зелений » ясно-зелений Буряк червоний Томат червоний Гарбуз Кріп Хрін (корінь) Часник Черемша Шпинат
|
15 30 25 15 50 70 40 30 10 60 10 20 5 5
250 150 20 25 20 30 10 10 40 8 150 200 Сліди 40 50 |
Абрикоси Апельсини Кавуни Барбарис Брусниця Виноград Вишня Голубика Гранат Грейпфрут Груша Диня Ожина Суниця лісова » садова Калина Кизил Журавлина свіжа » залежана » підсніжна Агрус Лимон Малина Мандарини » кірка Морошка Горіх волоський зелений Смородина біла » червона » чорна Черемха Чорниця Шипшина, сушена ціла, плоди червоного кольору Шипшина, сушена плоди темно забарвлення Яблука тітовка, антонівка Яблука різні
|
7 40 7 150 15 3 15 20 5 40 4 20 5 30 60 70 50 10 0 0 50 40 30 30 100 30 1200 5 30 300 Сліди 5 1500
100
30
7 |
ДОДАТОК Г
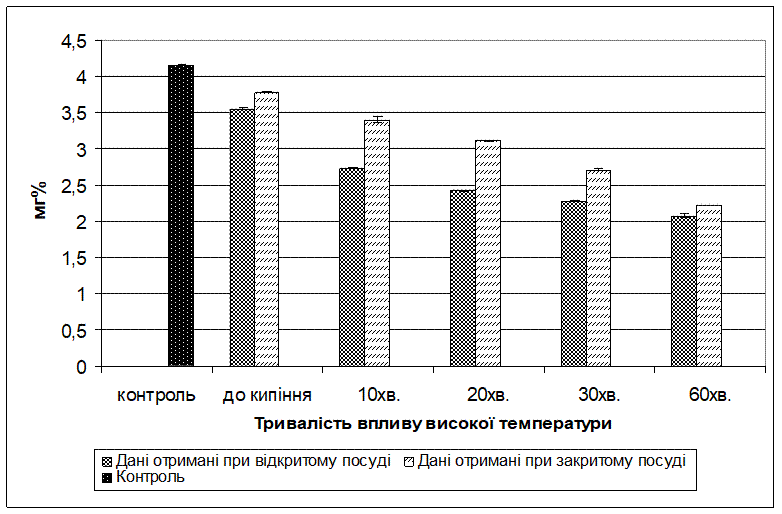
Рис. 3.1. Динаміка зміни вмісту вітаміну С в бульбах картоплі при дії високої температури в закритому і відкритому посуді
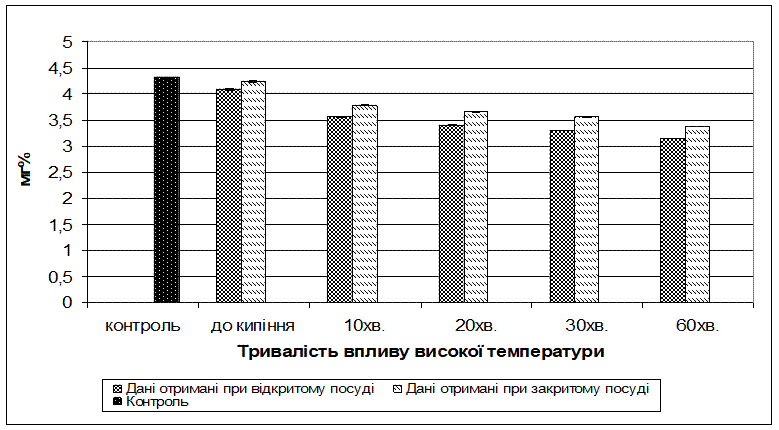
Рис. 3.2. Динаміка зміни вмісту вітаміну С в білокачанній капусті при дії високої температури в закритому і відкритому посуді
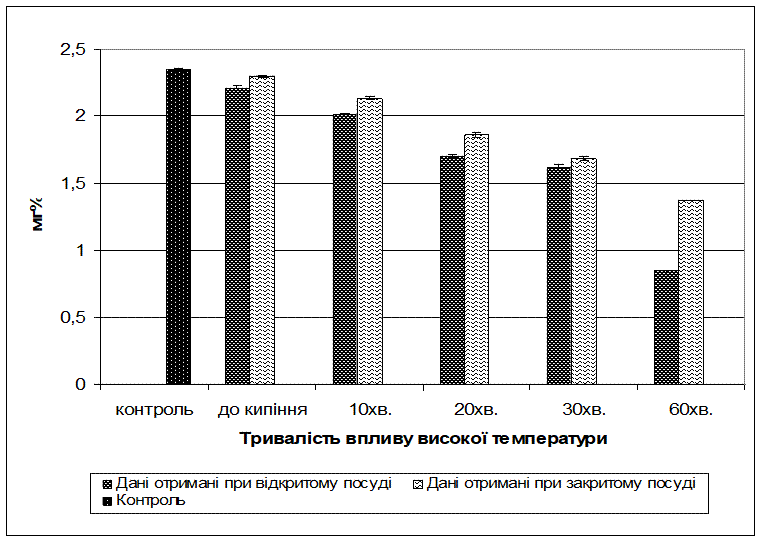
Рис. 3.3. Динаміка зміни вмісту вітаміну С в яблуках сорту «Лігольд» при дії високої температури в закритому і відкритому посуді
Редакція може не поділяти думку авторів і не несе відповідальність за достовірність інформації. Будь-який передрук матеріалів з сайту може здійснюватись лише при наявності активного гіперпосилання на e-kolosok.org, а також на сам матеріал!